湖州申科构建了覆盖全领域、全场景的支原体检测一站式合规解决方案。产品矩阵丰富,包括支原体 DNA 提取纯化试剂盒(2G)、检测试剂盒(2G,PCR - 荧光探针法)、DNA 校准品、一体化检测卡盒、外源因子全自动核酸分析系统,以及 10 余种支原体验证菌株(已上市猪鼻、肺炎、口腔支原体等,即将上市发酵、精氨酸支原体等)。方案具备极强的场景适配性,可应对 5% 人白、高浓度细胞等复杂基质样品,支持从起始材料到终产品的全流程检测,满足细胞疗法、抗体、疫苗、CRO/CDMO 等不同领域的检测需求。服务层面,提供从方法学建立、样品检测、适用性验证、传统法与 qPCR 法比对到特殊菌株定制的全流程技术支持,配合企业完成监管机构现场审计,满足企业从 IND 到 BLA/NDA 的申报需求,实现 “极简操作、一步加样、避免污染、全量检测” 的价值。
支原体检测NAT法(核酸扩增法)周期只需 3-6 小时,灵敏度高、特异性强,是生物制品快检优先选择方案。上海免疫细胞产品支原体检测核酸扩增法
湖州申科 MycoSHENTEK® 支原体检测解决方案以合规性为中心,具备突出的验证优势。该方案的试剂盒已完成 FDA 的 DMF 备案,经过 FDA 严格审核确认准确性与合规性,企业可直接引用备案信息,简化海外申报流程,降低审查不确定性,减少材料准备周期。方案通过了与合规机构的三方验证,联合合规机构获取标准菌株盘、建立 GC 比检测方法,共同开展提取效率验证、引物设计优化、反应体系与仪器程序开发,并由合规机构指导参与室间验证及检测限、专属性、耐用性等关键性能验证,严谨性与专业性获得行业认可。此外,方案还能为企业提供 NDA/BLA 申报验证支持,降低申报风险,同时涵盖试剂盒、设备、菌株、检测验证服务、现场审计等全流程服务,一站式解决企业整合成本高、流程复杂的痛点。
上海免疫细胞产品支原体检测核酸扩增法rHCDpurify 前处理系统可自动化提取支原体 DNA,减少人为误差提升批间稳定性。
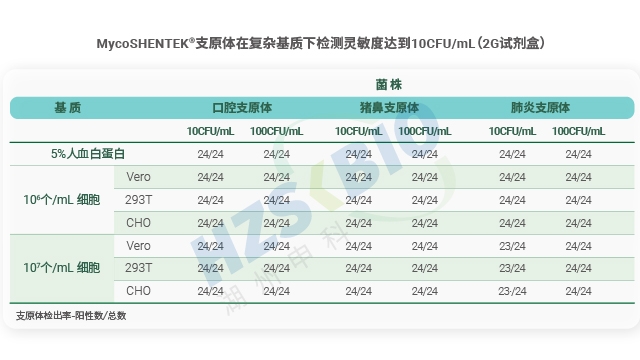
检测限验证是支原体 NAT 方法(核酸扩增法)合规性的关键要求,法规明确界定需为每种目标支原体确定阳性检测临界值。验证流程需满足严格的实验设计:每种支原体至少进行三次单独的 10 倍梯度稀释,每次稀释后需制备平行管检测,再确保各稀释浓度获得 24 个检测结果。阳性临界值的判定标准为,该浓度下至少 95% 的试验运行能得到阳性结果,即 24 个样品中需至少出现 23 个有效阳性结果。这一严谨设计旨在确保 NAT 检测方法在实际应用中,能够稳定检出低浓度支原体污染,避免因检测灵敏度不足导致的安全风险,为生物制品质量控制提供可靠保障。
全球主流药典均认可 NAT 法作为支原体检测的替代方法,但明确要求需经过充分验证并证明与传统方法的可比性。欧洲药典(EP)2.6.7 规定 NAT 法可作为替代方法,需开展供试品抑制性验证;美国药典(USP)63&77 要求替代方法需与培养法、指示细胞培养法均具备可比性,且 USP<77> 专门针对支原体 NAT 法的验证与检测制定了规范;日本药典(JP)G3-14-170 允许经适当验证后的 NAT 法替代传统方法;中国药典 3301 及相关指导原则明确,CAR-T、干细胞等新型产品可采用 NAT 法,但需充分验证其最低检出限不低于药典方法,早期需与药典方法并行使用。此外,各国法规均强调,NAT 法的选择、开发与应用需基于科学依据,充分考虑培养基、生产工艺、潜在污染菌株等因素。
复杂基质样品(如10⁷细胞、5%人白)检测中,MycoSHENTEK支原体检测试剂盒抗干扰能力突出。
2023 年美国国立卫生研究院(NIH)的对比研究得出一个结论是并非所有商业化支原体检测试剂盒都能满足替代传统方法的要求,研究对市面上 5 款主流试剂盒(ATCC、梅里埃、赛默飞、罗氏、MB)进行测试,发现不同试剂盒对不同支原体菌株的检测灵敏度差异明显,部分产品无法达到宣称的≤10 CFU/mL 检测限(符合欧、日药典替代培养法的要求)。例如,ATCC 试剂盒对莱氏无胆甾原体、精氨酸支原体的检测限只为 100 CFU/mL,MB 试剂盒对硬蜱螺原体无法检出(>1000 CFU/mL)。这一现象表明,试剂盒的检测性能与支原体菌株特性密切相关,因此企业需根据待测样品的原辅料来源和检测目的,对试剂盒进行严格的性能验证,避免因检测限不达标导致质量风险。
全血基质中100 CFU/mL支原体,湖州申科支原体检测试剂盒通过优化提取流程实现稳定扩增与检出。浙江重组药物支原体检测方法学验证
湖州申科提供支原体检测 qPCR 法方法学验证服务,含检测限、专属性、可比性等全维度验证。上海免疫细胞产品支原体检测核酸扩增法
湖州申科构建了具有完备资质的支原体技术服务平台,为企业提供多元化支持。平台拥有 BSL-2/P2 微生物实验室备案资质,遵循 GMP-like 质量体系,具备支原体培养法、指示细胞法与 qPCR 法的检测及验证能力,配备符合药典要求的支原体标准菌株库与高灵敏度培养基(含液体、固体、半流体)。企业已通过 ISO13485:2016 质量管理体系认证(证书号 MD 709873),检测中心获得 CNAS 认证(注册号 CNAS L21942),符合 ISO/IEC 17025:2017 标准,具备国际互认资质。平台可提供多元化技术服务,包括支原体 qPCR 法检测能力建立、实验员能力考核、质量体系与流程搭建、实验室设计方案优化,以及样品检测(三种方法)、样品适用性验证、方法学验证、传统法与 qPCR 法比对、特殊菌株定制生产等,申报阶段可配合客户与监管机构完成现场审计。
上海免疫细胞产品支原体检测核酸扩增法