MDCK(Madin-DarbyCanineKidney,马丁达比犬肾上皮细胞)细胞系是源于犬肾的持续性细胞系,广泛应用于流感病毒增殖纯化、流感疫苗生产等过程,作为细胞基质使用。凭借高病毒产量与滴度、无适应性突变、易驯化等优势,MDCK细胞已成为业界公认的流感病毒毒株分离及流感疫苗生产适配细胞系。和其他产品杂质类似,MDCK宿主残留蛋白(HCP)可能对生物制品的安全性与有效性产生不良影响,因此在生产监测、产品放行等环节,需对其开展定量研究并实施严格控制。SHENTEK®MDCK HCP残留检测试剂盒(一步酶联免疫吸附法),是湖州申科生物自主研发、拥有完全自主知识产权且关键试剂实现全国产化的MDCK HCP通用检测试剂盒。该试剂盒适用于基于MDCK细胞基质的病毒增殖纯化、疫苗生产等过程,可对其中的MDCK宿主残留蛋白进行定量检测,且操作步骤简便快捷、检测专一性高、性能稳定可靠。
定制化宿主细胞蛋白残留检测试剂盒产生的HCP抗体特异性更好,能检出高风险HCP。江苏Vero宿主细胞蛋白(HCP)残留检测
LC-MS技术作为生物制品宿主细胞蛋白(HCP)残留检测的新趋势,应用时需重点考虑以下五方面:①稳定性:需对HCPs的LC-MS检测流程开展验证,全流程需实施严格QC管控,以保障检测结果的一致性与稳定性。②可重复性:不同类型生物制品中HCPs的提取效率存在差异,且不同人员操作会产生偏差,因此需在上机前通过多种方法评估HCPs提取效率,规避人为因素导致的结果重复性不佳问题。③准确度:在方法开发与验证阶段,需设置内标并确定定量算法,通过内标响应回算得出HCPs含量,以此保证定量结果的准确性。④抗干扰能力:高丰度蛋白与特殊基质会干扰质谱检测,需借助前处理手段去除高丰度蛋白或特殊基质,从而降低其对HCPs肽段质谱检测的影响。⑤真实性:样品中除HCPs外的其他物质在质谱分析中也会产生质谱信号,需去除复杂背景噪音以避免假阳性与假阴性情况,同时建立规范的生信分析流程。在分析流程搭建过程中,同样需制定严格的QC标准,并通过后续多种方法验证,明确该标准的真实性。
广东定制化宿主细胞蛋白(HCP)残留检测围绕 HCP 检测试剂盒开发,需统筹法规适配、物料稳定、团队专业响应及案例积累,构建体系化保障体系。
宿主细胞蛋白(HCP)多与细胞关键功能相关,像细胞增殖、基因转录、蛋白合成修饰、细胞存活及凋亡等,工艺过程中会通过细胞分泌,或因细胞死亡、裂解而释放。生产环节中,主要有三方面因素影响HCP的组成与丰度:①宿主细胞基因组调控及培养工艺:特定工艺下潜在HCP数量可能极多,且并非所有基因都会表达,部分基因的表达存在时间与条件差异;例如大肠杆菌约含4300个基因,不同工艺产物会经历独特的翻译后修饰,增加HCP的总数与生化复杂性。研究表明,大肠杆菌表达的蛋白存在数量差异,这可能是对环境条件的适应性反应,但85-90%有潜在免疫原性的HCP在不同发酵过程中均会出现。②产物表达方式:宿主细胞与外源基因、载体及辅助成分构成的体系,可实现稳定、瞬时及诱导表达;以大肠杆菌为例,常见的表达形式包括胞内表达、分泌表达、可溶性表达、不溶性包涵体形式,以及融合与非融合表达。③纯化步骤及产品自身特性:纯化过程中能去除99%以上的HCP,但仍有残留HCP保留在产品中,这些残留HCP可能与产品结合,随产品一同完成纯化。
湖州申科在宿主细胞蛋白(HCP)ELISA 检测技术领域具备深厚技术积累,已成功搭建高质量全流程自有开发平台,覆盖 HCP 检测试剂盒研发的关键环节:①抗原表征与制备:依托合规平台的 HCP Reference/Antigen 制备能力,采用 2D 凝胶电泳等先进技术保障抗原库的代表性;②动物免疫与抗体制备:凭借自有免疫动物平台,把控免疫原设计及动物免疫流程,获得高特异性、广覆盖度的抗体;③体系开发与验证:借助成熟技术经验开发高灵敏度、高稳定性检测体系,且严格依照 GMP 标准完成方法学验证。该平台通过全流程自主可控的技术整合,从源头保障试剂盒性能的一致性与可靠性,降低不同批次试剂盒的检测变异性。其研发的 HCP ELISA 试剂盒已成功为国内外 200 余家生物医药企业提供服务,为单抗、疫苗等生物制品的工艺开发、质量控制及 IND/BLA 等法规申报,提供符合监管要求的定制化检测解决方案。
定制化宿主细胞蛋白残留检测试剂盒抗原校准品更具代表性,减少HCP漏检和定量误差。
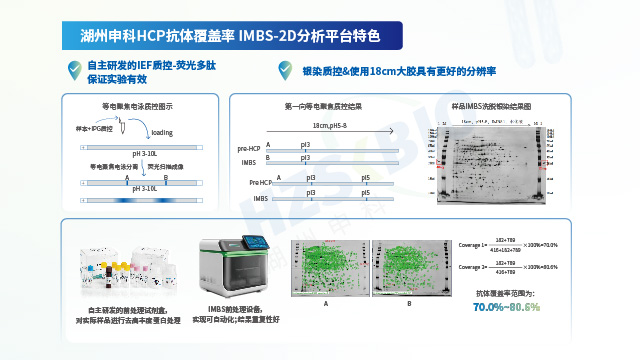
湖州申科运用免疫磁珠分离技术(IMBS),搭配 2D 电泳或 LC-MS 技术评估抗体覆盖率。IMBS 的主要流程涵盖:多克隆抗体与磁珠的偶联反应、磁珠未结合位点的封闭处理、HCP 样本与结合抗体的磁珠共同孵育反应。该过程中,HCP 抗体会结合可识别的 HCP,未被识别的 HCP 则通过后续洗涤步骤去除,随后借助低 pH 等洗脱条件,收集抗体捕获的 HCP。此方法具备 AAE(抗体亲和提取,Antibody Affinity Extraction)免疫层析柱分离的全部优势,同时免疫磁珠可在悬浮状态下与 HCP 样品充分混匀并结合,HCP 结合效果更优;且依托磁珠吸附,能减少 HCP 与填料的非特异性吸附,进一步提升实验准确性。
部分数据表明,定制化HCP检测试剂盒的检测准确度比商业化试剂盒高,更能满足产品质量控制所需。
广东定制化宿主细胞蛋白(HCP)残留检测HCP检测的经典方法是ELISA法,但该方法在检测过程中存在漏检风险,需要对试剂盒抗体进行抗体覆盖率评估。江苏Vero宿主细胞蛋白(HCP)残留检测
全球范围内快速增长的抗体、蛋白类等生物药,均由对应的工程细胞生产制备。在生物制品生产流程中,宿主细胞产生的内源性蛋白(即宿主细胞蛋白,Host Cell Proteins, HCPs),会随不同工艺环节部分残留在终产品中。HCPs 作为外源蛋白,可能在不同程度上诱发机体免疫应答,进而引发过敏反应或其他不良反应;此外,部分残留 HCPs 具备蛋白酶或脂酶活性,可能造成蛋白药物或辅料降解,从而加大药物质量与疗效的不稳定性。基于上述风险,对药物中 HCPs 开展定性与定量检测至关重要。全球主要药典(如美国药典、欧洲药典、中国药典)均针对 HCPs 检测制定了具体要求与标准。
江苏Vero宿主细胞蛋白(HCP)残留检测