支原体检测中,污染引发的假阳性是生物制品企业的痛点。实验室环境控制不当、人员操作不规范、仪器耗材混用等因素,都可能导致核酸气溶胶污染或上样污染,进而影响检测结果。一旦出现假阳性,企业需花费大量时间排查验证,严重时会导致批次报废、影响其他产品正常生产。常规 NAT 检测法虽比传统培养法快速,但仍存在明显短板:需配备前处理设备、PCR 仪器等多重耗材,核酸提取、PCR 上机、高浓度产物处理等多个环节均有污染风险;实验准备需 40-60 分钟,操作耗时超 4 小时,每天只能完成 1-2 轮单一类型样本检测,且对场地和人员技能要求极高,需单独划分试剂准备区、样品制备区等多个区域,人力与场地成本高昂。
支原体检测是生物制品质量控制的关键环节,需兼顾合规性与检测效率。浙江免疫细胞产品支原体检测可比性验证
支原体是一类无细胞壁的原核微生物,直径只有 0.1-0.8 µm,常规 0.22 µm 细菌过滤器无法有效去除,其污染在细胞培养领域极为普遍。这类微生物会严重干扰培养细胞的表型特征与正常生长,给生物制品质量安全带来极大隐患,且与细菌、真菌污染不同,支原体污染通常不会导致培养液浑浊或细胞可见病变,需通过专业方法检测。基于此,FDA、WHO 等全球监管机构及 USP、EP、ChP 等主流药典均明确要求,对测试细胞库(主细胞库、工作细胞库)、下游细胞培养物、终产品及对照细胞等关键环节开展支原体污染筛查,确保生物制品生产全流程安全可控。
福建重组药物支原体检测试剂盒支原体兼具胞内胞外生存特性,检测需裂解细胞而非只取上清,避免漏检胞内污染。
湖州申科构建了具有完备资质的支原体技术服务平台,为企业提供多元化支持。平台拥有 BSL-2/P2 微生物实验室备案资质,遵循 GMP-like 质量体系,具备支原体培养法、指示细胞法与 qPCR 法的检测及验证能力,配备符合药典要求的支原体标准菌株库与高灵敏度培养基(含液体、固体、半流体)。企业已通过 ISO13485:2016 质量管理体系认证(证书号 MD 709873),检测中心获得 CNAS 认证(注册号 CNAS L21942),符合 ISO/IEC 17025:2017 标准,具备国际互认资质。平台可提供多元化技术服务,包括支原体 qPCR 法检测能力建立、实验员能力考核、质量体系与流程搭建、实验室设计方案优化,以及样品检测(三种方法)、样品适用性验证、方法学验证、传统法与 qPCR 法比对、特殊菌株定制生产等,申报阶段可配合客户与监管机构完成现场审计。
AdvSHENTEK外源因子全自动核酸检测分析系统以 “迷你 qPCR 实验室” 的创新形态,突破了传统支原体检测的场地限制。整套系统尺寸为 380mm×305mm×343mm,重量只有 14kg,体积小巧、易于部署,无需专门的 PCR 实验室,只需一间普通实验室即可满足检测需求,大幅降低了企业的场地投入成本。这与传统 NAT 法需严格划分试剂准备区、样本制备区、扩增区等多个功能区域的要求形成鲜明对比,尤其适合场地资源紧张的中小企业。同时,系统一体化设计减少了耗材搭配与损耗,自动化流程降低了人为操作失误导致的重复检测成本,从场地、人力、耗材多维度为企业实现降本增效,让支原体检测更具经济性。
支原体检测 NAT 法引物设计需平衡覆盖范围与特异性,避免交叉反应。
此前,支原体检测依赖培养法和指示细胞培养法,这两种传统方法均被各国药典列为基础检测手段,但存在明显短板。培养法作为 “金标准”,需阳性活菌参照,每批次培养基需做灵敏度测试,完整合规检测周期长达 21-35 天;指示细胞培养法同样耗时 14-28 天,难以满足新型生物制品快速上市、短货架期的放行需求。更棘手的是,面对高蛋白等复杂样品基质,传统方法易受干扰或抑制,需额外增加传代培养步骤,导致检测时间再延长 2-3 周,严重影响生产效率,也难以适配新型生物制品的检测场景。
支原体检测试剂盒需覆盖常见污染菌株,避免因菌株遗漏导致漏检。湖南复杂基质支原体检测NAT法
疫苗病毒种子批支原体检测需取全量样品,建议进行 10mL 种子液提取,确保无漏检。浙江免疫细胞产品支原体检测可比性验证
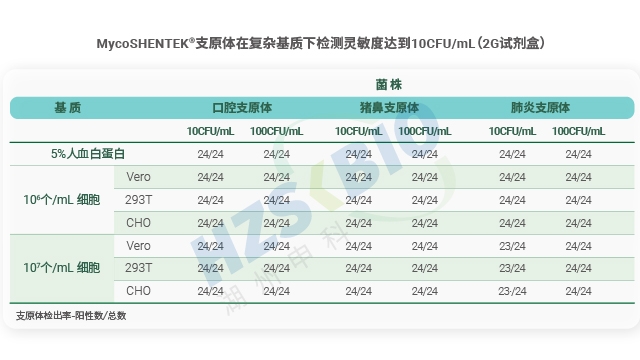
检测限验证是支原体 NAT 方法(核酸扩增法)合规性的关键要求,法规明确界定需为每种目标支原体确定阳性检测临界值。验证流程需满足严格的实验设计:每种支原体至少进行三次单独的 10 倍梯度稀释,每次稀释后需制备平行管检测,再确保各稀释浓度获得 24 个检测结果。阳性临界值的判定标准为,该浓度下至少 95% 的试验运行能得到阳性结果,即 24 个样品中需至少出现 23 个有效阳性结果。这一严谨设计旨在确保 NAT 检测方法在实际应用中,能够稳定检出低浓度支原体污染,避免因检测灵敏度不足导致的安全风险,为生物制品质量控制提供可靠保障。
浙江免疫细胞产品支原体检测可比性验证