中药作为我国传统医学的瑰宝,拥有丰富的资源,但在现代化发展过程中面临着成分复杂、作用机制不明确等挑战。环特药物筛选为中药现代化提供了有力的技术支持。通过将中药提取物或单体化合物应用于斑马鱼模型,可以快速评价其药效和安全性。例如,在研究中药的抑炎作用时,利用斑马鱼炎症模型,观察中药处理后炎症相关指标的变化,如炎症细胞浸润、炎症因子表达等。同时,结合高通量测序技术,分析中药对斑马鱼基因表达的影响,揭示其抑炎作用的分子机制。环特药物筛选能够帮助筛选出中药中的有效成分,优化中药配方,提高中药的质量和疗效,推动中药走向国际市场,实现中药现代化和国际化的发展目标。基于类organ技术,环特生物升级药物筛选体系,贴近人体生理状态。活性筛选评价委托

体内筛选通过构建动物影响或tumor移植模型,更真实地模拟药物在体内的代谢过程及宿主-病原体相互作用。在细菌耐药研究中,小鼠腹膜炎模型是常用体系。例如,将金黄色葡萄球菌接种至小鼠腹腔,随后腹腔注射万古霉素,连续医疗14天后分离肝脏和脾脏中的存活菌株,发现dltABCD基因簇突变导致细胞壁负电荷减少,是万古霉素耐药的重要机制。在tumor耐药领域,患者来源tumor异种移植(PDX)模型因其保留原始tumor的异质性和微环境特征而备受关注。例如,将非小细胞肺ancer患者的tumor组织移植至免疫缺陷小鼠,经奥希替尼医疗8周后,tumor体积缩小50%但后续复发,基因测序显示复发灶中EGFRC797S突变频率从0.1%升至35%,揭示了第三代EGFR-TKI耐药的新机制。活性筛选评价委托斑马鱼实验助力中药成分筛选,环特生物推动中医药现代化研发。

当前耐药株筛选面临三大挑战:一是模型与临床的差异,体外筛选可能忽略宿主免疫和药物分布的影响;二是耐药机制的复杂性,同一病原体可能通过多基因协同或表观遗传调控获得耐药性;三是筛选效率与成本的平衡,高通量技术虽能加速筛选,但数据解读和验证仍需大量资源。未来发展方向包括:一是构建更贴近临床的模型,如人源化小鼠模型或器官芯片技术;二是发展多组学整合分析平台,结合机器学习预测耐药突变热点;三是探索耐药株的“合成致死”策略,即利用耐药株的特定缺陷开发针对性的药物。例如,在BRCA突变型卵巢ancer中,PARP抑制剂通过合成致死效应杀伤肿瘤细胞,而耐药株常因53BP1表达缺失恢复同源重组修复能力,针对这一机制开发53BP1激动剂可逆转耐药。随着技术的不断进步,耐药株筛选将为精细医疗和耐药防控提供更强有力的支持。
药物组合筛选面临三大关键挑战:一是组合空间性增长(如100种药物的两两组合达4950种,三三组合达161700种),导致实验成本与周期难以承受;二是药代动力学(PK)与药效动力学(PD)的复杂性,不同药物吸收、分布、代谢及排泄的差异可能削弱体内协同效应;三是临床转化率低,只约10%的体外协同组合能在体内验证有效。针对这些挑战,优化策略包括:1)采用智能算法(如机器学习、深度学习)预测潜在协同组合,缩小实验范围。例如,基于药物化学结构、靶点信息及疾病基因组数据构建预测模型,可优先筛选高概率协同组合;2)开发微流控芯片或器官芯片技术,模拟体内动态环境,实时监测药物组合的PK/PD过程,提高体外-体内相关性;3)建立多阶段筛选流程,先通过高通量细胞实验快速筛选,再利用类organ或动物模型验证,进行临床试验,逐步淘汰无效组合,降低研发风险。药物筛选是从海量化合物中准确找出有潜在药效物质的关键步骤。
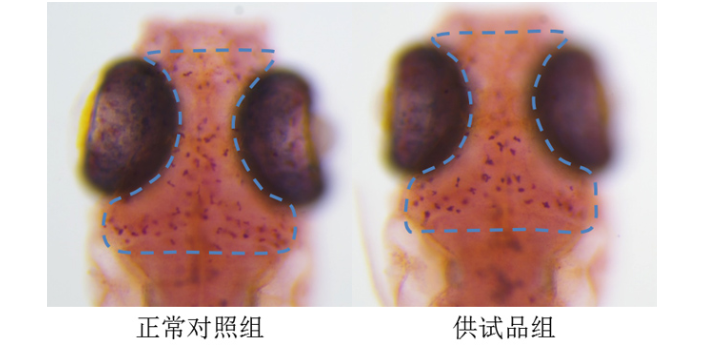
环特生物的药物筛选技术已推动多个新药项目进入临床试验阶段。例如,其与奥默药业合作研发的新型肌肉松弛拮抗药物,通过斑马鱼类过敏检测发现Bridion在高剂量下的致敏性,经结构优化后已进入III期临床试验;北京市tumor研究所基于环特转基因斑马鱼模型发现的多肽药物,亦已完成临床前研究并提交IND申请。此外,环特的技术平台已服务赛诺菲、药明康德等100余家国内外药企,申请发明专利57项,发表SCI论文98篇,其斑马鱼实验数据被广泛应用于CFDA/NMPA的临床试验申报。未来,环特将继续深化类organ、环肽及AI驱动的药物筛选技术研发,为全球新药研发提供更高效的解决方案。药物筛选需结合多种技术手段,综合评估化合物的药用潜力。活性筛选评价委托
创新药物筛选阶段,环特生物提供早期毒性评估,规避研发风险。活性筛选评价委托
尽管前景广阔,药物组合筛选仍面临多重挑战:一是实验复杂性,和药物相互作用可能随剂量、时间、细胞类型变化,需设计动态监测系统(如实时细胞成像、单细胞测序)捕捉动态效应;二是临床转化瓶颈,动物模型与人体环境的差异可能导致体外协同效应在体内失效,需开发更贴近生理条件的3D组织模型或类organ平台;三是数据整合难题,高通量筛选产生的海量数据(如细胞活性、基因表达、代谢组学)需通过AI算法挖掘隐藏的协同模式,例如深度学习模型可预测药物组合对特定患者亚群的疗效。未来,药物组合筛选将向“精细化”和“智能化”发展:结合患者基因组、蛋白质组数据定制个性化组合方案,利用器官芯片技术模拟人体organ间的相互作用,终实现从“经验性联用”到“基于机制的精细组合”的跨越,为复杂疾病医疗开辟新范式。活性筛选评价委托