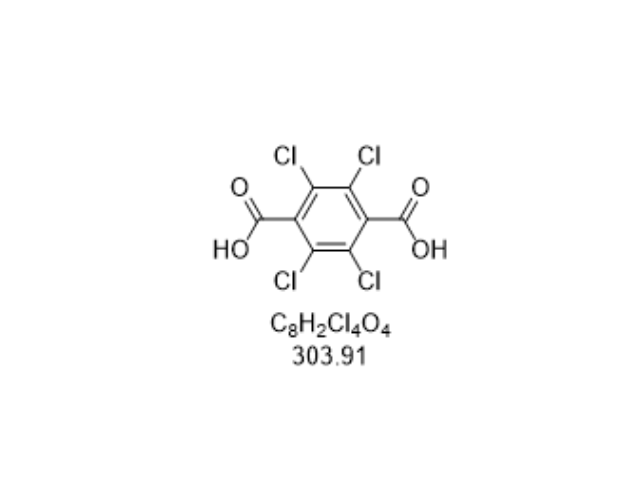
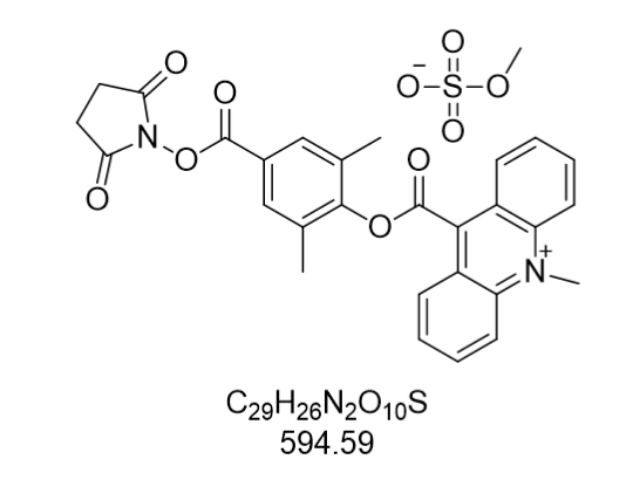
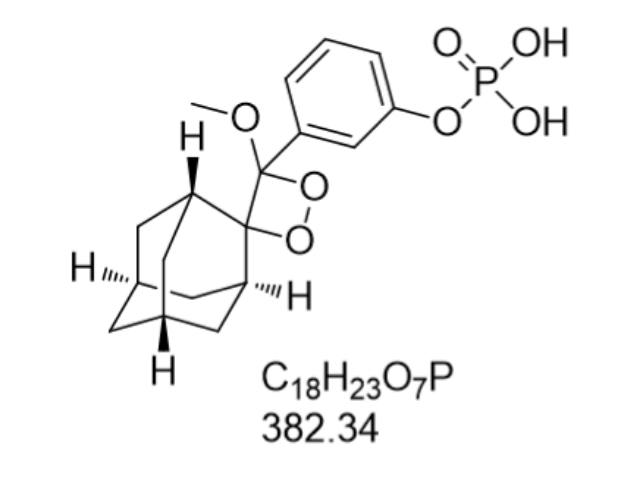
- 品牌
- 同顺生物
紫杉醇不仅因其明显的抗疾病效果而备受瞩目,还因其独特的化学结构和作用机制成为科学家们研究的热点。作为一种二萜生物碱类化合物,紫杉醇具有新颖复杂的化学结构,其普遍而明显的生物活性以及全新独特的作用机制,使其在临床上具有不可替代的地位。它通过与微管蛋白的结合,抑制微管的分解,从而阻断疾病细胞的正常分裂过程。同时,紫杉醇还能直接与内质网结合,刺激钙释放到细胞质中,有助于诱导细胞凋亡。这些独特的药理作用使得紫杉醇在疾病医治中发挥着重要作用。由于其自然资源的奇缺和提取工艺的复杂性,紫杉醇的生产成本较高,限制了其普遍应用。因此,科学家们正在积极寻找和开发紫杉醇的替代药物或合成方法,以期能够降低生产成本,提高其在疾病医治中的可及性和疗效。监管部门定期对原料药企业开展飞行检查,强化质量监管。陕西硼替佐米
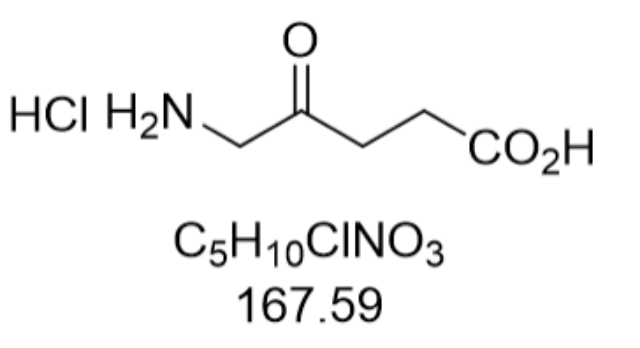
全球原料药贸易格局正经历深度调整,2020年以来,印度作为全球较大的原料药出口国,因疾病导致的工厂停工曾引发全球抗疟药等关键品种的供应危机,这促使欧盟、美国等发达经济体加速构建战略原料药储备体系。中国原料药出口则面临更复杂的挑战,一方面,人民币升值、原材料价格上涨等因素压缩了传统大宗原料药的利润空间;另一方面,欧美市场通过FDA检查频次增加、DMF文件审核趋严等手段设置技术壁垒。在此情境下,中国企业的应对策略呈现两极分化:大型企业通过并购海外工厂实现本地化生产,如华海药业在美国新泽西州建立的制剂工厂可直接配套原料药供应;中小型企业则转向特色原料药领域,聚焦抗疾病、抗糖尿病等高技术门槛品种,通过差异化竞争获取市场空间。值得注意的是,RCEP协定的实施为亚太地区原料药贸易创造了新机遇,区域内关税减免和原产地规则优化有望促进产业链区域化整合。陕西硼替佐米原料药的生产过程控制需严格,确保产品质量一致。
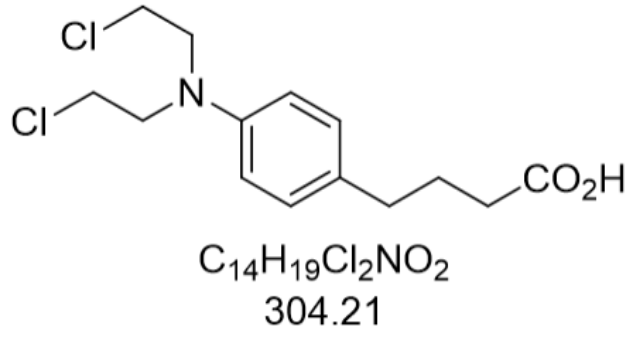
在多发性骨髓瘤的医治体系中,美法仑的地位经历了从单药医治到联合方案的演进。早期MP方案(美法仑+泼尼松)作为不适合大剂量化疗患者的标准医治,客观缓解率可达60%-70%,中位生存期延长至3-4年。随着新型药物的出现,美法仑逐渐转向特定场景应用:在自体移植预处理中,其与环磷酰胺、白消安的联合方案可使完全缓解率提升至85%以上;对于老年或肾功能不全患者,含美法仑的减量方案(如美法仑50 mg/m²+来那度胺)仍能维持50%以上的缓解率。临床研究显示,接受美法仑预处理的患者,其移植后中性粒细胞植入中位时间为11天,血小板植入为13天,明显快于非烷化剂方案。然而,肾功能损害患者的剂量调整至关重要——当血尿素氮(BUN)≥30 mg/dL时,姑息医治剂量需减半至8 mg/m²,否则可能引发尿毒症性骨髓抑制。这种个体化剂量策略在四川汇宇制药2023年申报的注射用盐酸美法仑临床研究中得到验证,其III期试验纳入120例肾功能不全患者,调整剂量后严重骨髓抑制发生率从32%降至15%。
在临床应用层面,卡巴他赛的剂量方案经过严格优化。标准推荐剂量为25mg/m²每3周一次,或20mg/m²用于存在高危因素的患者。给药前需通过两步稀释法配制,并使用0.22μm在线过滤器持续灌注1小时以上,同时需预先给予抗组胺药、皮质类固醇和H2拮抗剂预防过敏反应。2021年法国古西塔夫·鲁西疾病研究所开展的随机对照试验中,195例未接受化疗的mCRPC患者中,43%明确偏好卡巴他赛作为医治,其重要优势在于明显降低疲劳发生率(72%)、改善生活质量评分(64%)及减少脱发等非血液学毒性。值得注意的是,该药物在肥胖患者中的剂量计算需基于实际体重,ASCO指南强调需以全重量计算体表面积,并在毒性缓解后恢复初始剂量。对于合并肝肾功能损害的患者,剂量调整策略尤为关键:中度肝损伤(总胆红素1.5-3倍ULN)患者需减量至15mg/m²,严重肝损伤(总胆红素>3倍ULN)则禁用;肾功能不全(CrCl<15mL/min)患者需密切监测并谨慎用药。原料药的生产工艺创新可提高产品纯度和收率。
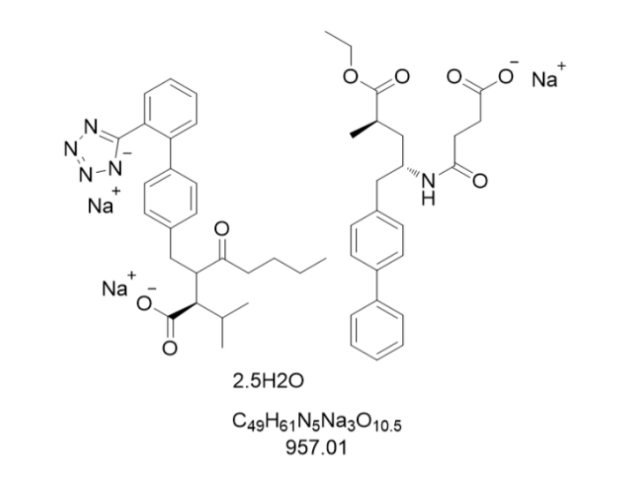
从临床应用性能评估,Ixazomib citrate的口服特性彻底改变了多发性骨髓瘤的医治模式。作为获批的口服蛋白酶体抑制剂,其每周一次的给药的方案明显提高了患者依从性,尤其适合老年或行动不便患者。真实世界研究显示,IRd方案的持续医治率达78%,较硼替佐米方案(42%)提升近一倍。在耐药患者中,Ixazomib仍能保持32%的客观缓解率(ORR),这与其对硼替佐米耐药相关β5亚基突变(如G322A)的交叉抑制作用有关。经济性分析表明,尽管Ixazomib单价较高,但因其减少住院需求(无需静脉给药)和降低严重不良反应发生率,整体医治成本较硼替佐米方案降低18%。此外,该药物已纳入中国医保目录,患者自付比例降至30%以下,明显提升了可及性。未来研究方向包括探索Ixazomib在淀粉样变性、华氏巨球蛋白血症等蛋白酶体过度启动相关疾病中的应用,以及开发纳米晶体等新剂型以进一步提高生物利用度。原料药进出口需符合两国药监部门法规,办理通关审批手续。陕西硼替佐米
原料药的生产过程自动化可提高生产效率,减少人为误差。陕西硼替佐米
从研发历程到市场布局,艾沙佐咪的商业化路径体现了创新药开发的典型特征,2011年获得FDA和EMA的孤儿药资格认定,2015年11月率先在美国获批上市,商品名Ninlaro®。截至2025年,其已在全球68个国家注册上市,2018年4月通过中国NMPA审批,商品名恩莱瑞®。生产环节采用两步合成法:首先通过硼酸酯化反应制备中间体MLN-2238,再经柠檬酸成盐获得产物。质量控制标准严格,要求单杂含量≤0.1%,总杂质≤1%,水分含量≤1%。2024年全球销售额突破12亿美元,其中中国区贡献占比达18%,武田中国联合中国疾病基金会推出的患者援助项目,已为超过3000例低收入患者提供药品支持。陕西硼替佐米
从药代动力学特性分析,多西他赛展现出独特的体内过程特征。其三室模型药代动力学参数显示,α相半衰期只4分钟,β相36分钟,γ相长达11.1小时,这种快速分布与长效滞留的组合使其在疾病组织中形成持续药物浓度。当以100mg/m²剂量静脉滴注时,血浆峰浓度可达3.7μg/mL,AUC为4.6μg/mL·h,总体去除率21L/h/m²。值得注意的是,该药物94-97%的高血浆蛋白结合率虽可能影响游离药物浓度,但临床前研究证实等糖皮质物质的预处理不会改变其蛋白结合特性。排泄途径方面,约75%的代谢产物经粪便排出,只6%通过肾脏排泄,这种非肾依赖性去除机制为肾功能不全患者提供了用药安全性保障。体外代谢实验...