- 品牌
- 上海司鼎生物科技有限公司
- 型号
- 型号齐全
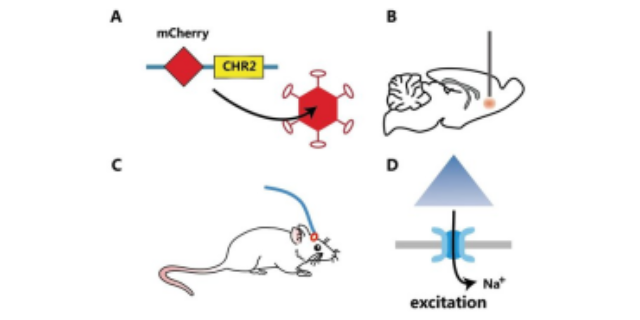
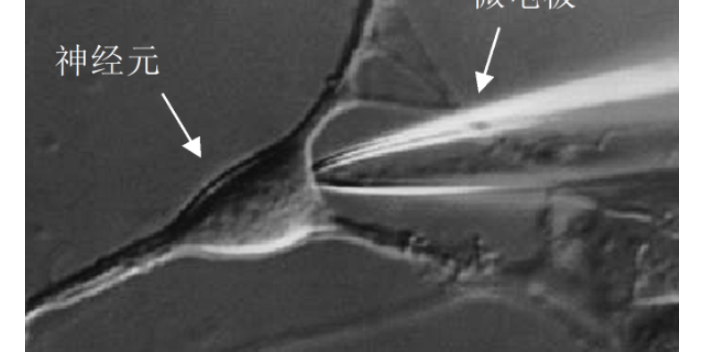
化学膜片钳技术方案融合化学调控与膜片钳记录两大重点要素,形成独特的技术原理体系。膜片钳技术通过玻璃微电极与细胞膜形成高阻抗封接,实现对细胞离子通道电流的高灵敏度检测,能够捕捉皮安级的微弱电信号变化,为研究细胞电生理特性提供精确数据。在此基础上,化学调控手段发挥作用,借助小分子化合物与细胞表面受体或离子通道的特异性结合,改变离子通道的开放概率和电导特性。这种结合可以是激动剂促使通道开放、拮抗剂阻断通道活性,或是调节剂改变通道动力学参数。通过化学物质的引入与膜片钳记录的同步进行,能够实时观察化学干预对细胞电活动的影响,从而在分子水平解析细胞电生理功能的调控机制,将化学信号与电信号的研究有机结合。光遗传技术是一种结合光学与遗传学手段的前沿科技,通过特定基因的编辑与表达,使细胞对光信号产生响应。光遗传技术用途
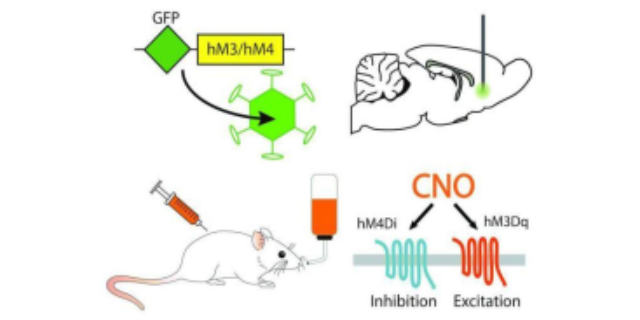
光遗传技术的重心在于将对光敏感的蛋白(如视蛋白)导入特定神经元中。当这些神经元表达视蛋白后,通过特定波长的光照射,就能精确控制神经元的活动。例如,向兴奋性神经元导入能被蓝光激发的通道蛋白,蓝光照射时,通道打开,阳离子内流,神经元兴奋。而化学遗传技术则是利用人工合成的配体与改造后的受体相互作用。将改造后的受体(DREADD)表达在目标神经元上,给予对应的配体(如 CNO),就能调控神经元的活性。这种技术能够在分子和细胞水平上,实现对神经元活动的精细调控,为神经科学研究提供了强大的工具。光遗传技术用途光遗传膜片钳技术服务通过技术融合展现出明显的创新价值。
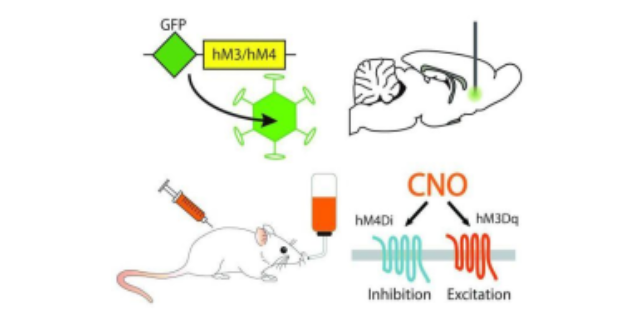
化学膜片钳技术方案具备多维度的明显优势。在实验可控性方面,化学物质的添加与去除能够灵活调节实验条件,可精确控制干预的时间节点和作用强度,相比传统电刺激等方式,能更细致地模拟生理或病理状态下的化学信号变化。在特异性上,随着小分子化合物研发技术的发展,越来越多具有高选择性的化学工具被应用,可针对特定类型的离子通道或受体进行作用,减少对其他细胞功能的干扰,提升研究结果的可靠性。此外,该方案能够兼容多种实验样本,无论是原代细胞、细胞系,还是脑片、心肌组织等,都能通过优化实验条件开展研究,同时可与其他技术如荧光成像、质谱分析等联用,从多层面获取细胞生理信息,为深入探究细胞功能提供系统的数据支撑。
化学遗传技术作为一种新兴的生物技术手段,具有诸多明显优势。首先,它通过改造生物大分子使其能够与特定的小分子相互作用,从而实现对生物大分子活性的可控、可逆调节。这种技术操作相对简单,实验要求较低,不需要复杂的设备支持,例如光遗传学所需的光纤和激光控制器。其次,化学遗传技术具有非侵入性特点,不会对实验动物造成额外的生理负担,尤其适合在自由活动状态下对神经元进行长期调控。此外,化学遗传技术的作用时程较长,能够实现数小时的持续赋活或抑制,这对于研究长期的神经环路调节具有重要意义。并且,化学遗传技术的安全性较高,常用的赋活剂如CNO是FDA批准药物的代谢产物,体内应用相对安全。这些优势使得化学遗传技术在生物医学研究中得到了普遍应用。化学膜片钳技术方案具备强大且多样化的功能特性。
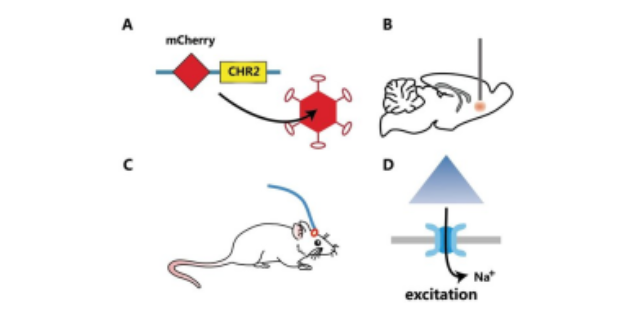
化学遗传技术方案在药物研发中具有重要价值。通过构建小分子-靶点相互作用模型,该技术能够快速筛选具有潜在生物活性的化合物,明显缩短药物发现周期。与传统高通量筛选方法不同,化学遗传技术可以基于靶点的三维结构信息,定向设计小分子配体,提高先导化合物的成药概率。此外,在药物作用机制研究方面,化学遗传技术能够实时追踪小分子药物与靶点结合后的动态变化,揭示药物发挥疗效的分子机制,为优化药物结构、提升药效提供关键依据,推动创新药物的开发进程。光遗传膜片钳技术平台整合了光遗传学与膜片钳技术的优势。光遗传技术用途
光遗传膜片钳技术服务构建了标准化的全流程服务体系。光遗传技术用途
光遗传技术需要精确的光学刺激系统来实现对光敏感蛋白的激发或抑制。典型的光学刺激系统包括光源、光纤和光电极等组件。光源通常采用激光或发光二极管(LED),它们能够产生特定波长和强度的光,以满足不同光敏感蛋白的需求。例如,对于 ChR2 激发,常使用 473nm 的蓝光激光,而对于 NpHR 抑制则采用 590nm 的黄光激光。光纤用于将光源产生的光传输到目标组织,其直径和数值孔径需根据实验需求进行选择,以确保光能够高效地传递到表达光敏感蛋白的细胞。光电极则可用于记录神经元的电活动,同时实现光刺激与电生理记录的同步,为研究神经元对光刺激的响应机制提供了更多方面的数据。这种精确的光学刺激系统使得研究人员能够在时间和空间上精确控制神经元的活动,深入探索神经信号传导的规律。光遗传技术用途
光遗传技术具有多项明显的优势,使其在生物医学研究中备受关注。首先,它能够实现对细胞活动的精确调控,通过光信号的精确控制,可以精确地赋活或抑制特定细胞,避免了传统方法中可能产生的非特异性影响。其次,光遗传技术具有高度的时空分辨率,可以在微秒级别的时间尺度上对细胞活动进行调控,同时可以在细胞水平上进行操作,实现对细胞活动的精确观察和分析。此外,光遗传技术还具有可逆性,通过光刺激的开启和关闭,可以实现对细胞活动的动态调控。这些优势使得光遗传技术在生物医学研究中具有广阔的应用前景。化学膜片钳技术方案具备多维度的明显优势。徐州光遗传膜片钳技术哪里有相较于传统电生理研究技术,光遗传膜片钳技术平台具有独特优...
- 南通化学遗传技术平台 2025-12-09
- 厦门化学膜片钳技术服务 2025-12-02
- 光遗传技术用途 2025-10-19
- 佛山化学遗传技术原理 2025-10-14
- 常州光遗传膜片钳技术哪家靠谱 2025-10-14
- 深圳化学遗传技术哪家靠谱 2025-06-08
- 南通光遗传技术哪里有 2025-06-07
- 芜湖化学膜片钳技术用途 2025-04-28
- 苏州光遗传技术原理 2025-04-07
- 常州光遗传膜片钳技术 2024-12-09
- 合肥化学膜片钳技术应用 2024-09-17
- 珠海光遗传膜片钳技术用途 2024-06-08


- 东莞组织芯片免疫荧光哪家专业 01-20
- 嘉兴细胞生物学膜片钳实验哪家好 12-23
- 南通化学遗传技术平台 12-09
- 厦门化学膜片钳技术服务 12-02
- 武汉组织芯片免疫组化用途 11-25
- 光遗传技术用途 10-19
- 佛山化学遗传技术原理 10-14
- 常州光遗传膜片钳技术哪家靠谱 10-14
- 苏州组织芯片免疫荧光哪家好 09-02
- 蚌埠多种位点组织芯片服务中心 08-09