- 产地
- 苏州
- 品牌
- 细胞高效转染试剂
- 型号
- 齐全
- 是否定制
- 是
影响转染试验的因素:细胞状态变化:(1)转染试剂与细胞不匹配细胞转染较适合的不是原代细胞,也不是传代很多次的细胞。这是因为细胞培养在实验室中保存数月和数年后会经历突变,总染色体重组或基因调控变化等而演化。这会导致和转染相关的细胞行为的变化。较适合转染的细胞是经过几次传代后达到对数生长期的细胞,细胞生长旺盛,较容易转染。(2)把握时机没错!转染也有适当的时机,相比较非分裂细胞——分裂细胞往往要比静止细胞更易于摄取并表达外源DNA。因此对大多数转染操作而言,细胞都在转染当天或前现在种板。同样重要的是细胞在种板进行转染时不应处于过度生长的状态,如细胞数量过多,互相叠加,营养物质耗竭,代谢废物积聚,转染率低下也是很正常的!对大多数细胞而言,均需要在转染当天或前现在铺板,第二天上午进行转染。金华正规细胞高效转染试剂平均价格

瞬时转染和转染效率的监测:基因的瞬时表达在24-72小时内就结束了。这种快速的瞬时表达非常适用于验证质粒表达和监测转染步骤的效率。可以使用报告基因来确定优化条件,其表达蛋白易检测,在目的细胞中不含此蛋白或水平很低。常用的报告基因包括氯霉素乙酰转移酶(CAT),绿色荧光蛋白(GFP),荧光素酶(Lux或Luc)以及b-半乳糖苷酶(b-gal)。可以使用简单的非同位素方法检测b-gal的表达以测定转染效率和活性。pCMVSPORT-bgal质粒包含CMV启动子调控下的LacZ基因,转染入真核细胞内后可以直接表达bgal。结合简单的检测步骤,可以做为监测转染条件的一种方便灵敏的方法。金华济南细胞高效转染试剂必须通过对药物的抗性筛选进行扩增或通过表型变化进行鉴定。

细胞转染,你至少要掌握以下几点:主要有下面几种方法::化学法:磷酸钙法、DEAE-右旋糖苷法、阳离子脂质体法;物理法:电穿孔法、显微注射法、颗粒传递法;细菌介导法:逆转录细菌、腺细菌A.阳离子脂质体法:带正电的脂质体与核酸带负电的磷酸基团形成复合物被细胞内吞。特点:简单通用,适用性广,转染效率高,重复性好,但转染时需除血清,转染效率随细胞类型变化大。由于脂质体复合物与贴壁细胞的接触机会远大于悬浮细胞,所以贴壁比悬浮转染效率要高。悬浮细胞建议使用电穿孔法。B.电穿孔法:利用高压电脉冲对细胞膜的干扰,使其形成利于核酸进入的微孔。
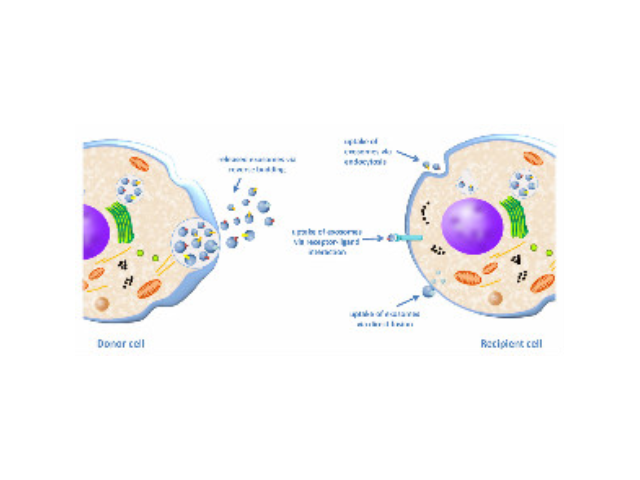
细胞转染的常用方法:人工脂质体法原理:带正电的脂质体与核酸带负电的磷酸基团形成复合物,进而可被细胞内吞稳定转染/瞬时性转染。这种方法几乎适用于所有细胞,转染效率高、重复型好,但转染时需要去除血清,转染效果随细胞类型变化大。实验步骤:在单独试管中分别稀释核酸及转染试剂→脂质体与核酸的磷酸骨架结合,形成复合物→脂质体上的正电荷有助于复合物与细胞膜结合→复合物通过内吞作用进入胞浆→分析细胞瞬时基因表达或沉默情况。来指示细胞中目标基因是否存在,这样的报告基因一般可以在转染后一两天内检测到。

细胞转染操作方法:转染,是将外源性基因导入细胞内的一种专门技术。随着基因与蛋白功能研究的深入,转染目前已成为实验室工作中经常涉及的基本方法。转染大致可分为物理介导、化学介导和生物介导三类途径。电穿孔法、显微注射和基因属于通过物理方法将基因导入细胞的范例;化学介导方法很多,如经典的磷酸钙共沉淀法、脂质体转染方法、和多种阳离子物质介导的技术;生物介导方法,有较为原始的原生质体转染,和现在比较多见的各种细菌介导的转染技术。理想细胞转染方法,应该具有转染效率高、细胞毒性小等优点。细菌介导的转染技术,是目前转染效率较高的方法,同时具有细胞毒性很低的优势。但是,细菌转染方法的准备程序复杂,常常对细胞类型有很强的选择性,在一般实验室中很难普及。其它物理和化学介导的转染方法,则各有其特点有血清时的转染 血清一度曾被认为会降低转染效率。济南细胞高效转染试剂平均价格
细胞易于生长到高密度并合成更多蛋白。金华正规细胞高效转染试剂平均价格
稳定转染细胞系的筛选:生长的细胞比不分裂的细胞更快的受到GENETICIN物品的影响。转染后,在开始筛选前等待48-72小时,使细胞表达足够量的抗性酶,保证在开始筛选时可以自我保护。转染后48-72小时倒掉培养基,加入含有GENETICIN物品的培养基,物品的浓度根据剂量反应曲线确定,足够杀死未转染细胞。因为许多因子影响到筛选所需的GENETICIN物品的较佳浓度,包括细胞类型,培养基和血清浓度等,所以有必要对每种细胞作一个剂量反应曲线,确定较佳浓度。筛选较多可能需要一周时间,因为在致死剂量的GENETICIN物品存在条件下,细胞会分裂1-2次。在次培养细胞时使用较低剂量的物品,一般是筛选剂量的一半。筛选后的细胞一般是离散的克隆,根据实验目的不同,可以分别纯化(克隆),收集进行大量培养或染色并进行抗性克隆的计数。金华正规细胞高效转染试剂平均价格
转染的注意事项:细胞铺板密度用于转染的较佳细胞密度根据不同的细胞类型或应用而异。一般转染时,贴壁细胞密度为70%-90%,悬浮细胞密度为2×106-4×106细胞/ml时效果较好。确保转染时细胞没有长满或处于静止期。因为转染效率对细胞密度很敏感,所以在不同实验间保持一个基本的传代步骤很重要。铺板细胞数目的增加可以增加转染活性和细胞产量。在三种不同密度进行细胞铺板的比较表明铺板密度较高的,CAT活性也较高。得到较高活性所需的LIPOFECTAMINE试剂的量也相应增加了。这些结果说明,对于转染相同量的DNA所需的较佳阳离子脂质体试剂的量会因细胞密度而异对于转染相同量的DNA所需的较佳阳离子脂质体...
- 北京细胞高效转染试剂平均价格 2026-05-19
- 徐州细胞高效转染试剂哪家便宜 2026-05-19
- 成都正规细胞高效转染试剂哪家便宜 2026-05-18
- 天津细胞高效转染试剂直销厂家 2026-05-18
- 天津正规细胞高效转染试剂厂家现货 2026-05-18
- 开封细胞高效转染试剂生产厂家 2026-05-18
- 郑州细胞高效转染试剂厂家 2026-05-18
- 金华重庆细胞高效转染试剂 2026-05-18
- 上海细胞高效转染试剂厂家推荐 2026-05-18
- 天津正规细胞高效转染试剂服务电话 2026-05-17
- 武汉正规细胞高效转染试剂价格 2026-05-16
- 无锡开封细胞高效转染试剂 2026-05-16
- 徐州细胞高效转染试剂报价 2026-05-16
- 重庆正规细胞高效转染试剂单价 2026-05-16
- 深圳细胞高效转染试剂单价 2026-05-16
- 太原正规细胞高效转染试剂平均价格 2026-05-16


- 宁波正规外泌体提取试剂哪家便宜 05-26
- 武汉RNA提取试剂哪家好 05-26
- 温州正规RNA提取试剂直销价 05-25
- 北京正规细胞外基质胶进货价 05-25
- 厦门正规无血清细胞冻存液厂家现货 05-25
- 广州细胞外基质胶哪里买 05-25
- 长沙正规外泌体提取试剂厂家现货 05-25
- 徐州原代细胞分离试剂盒平均价格 05-25
- 温州原代细胞分离试剂盒厂家推荐 05-25
- 天津外泌体提取试剂厂家推荐 05-25