- 品牌
- 司鼎;OriCell
聚合酶链式反应准备:PCR所用的酶主要有两种来源:Taq和Pfu,分别来自两种不同的噬热菌。其中Taq扩增效率高但易发生错配。Pfu扩增效率弱但有纠错功能。所以实际使用时根据需要必须做不同的选择。模板即扩增用的DNA,可以是任何来源,但有两个原则,纯度必须较高,第二浓度不能太高以免抑制。缓冲液的成分很为复杂,除水外一般包括四个有效成分:缓冲体系,一般使用HEPES或MOPS缓冲体系;一价阳离子,一般采用钾离子,但在特殊情况下也可使用铵根离子;二价阳离子,即镁离子,根据反应体系确定,除特殊情况外不需调整;辅助成分,常见的有DMSO、甘油等,主要用来保持酶的活性和帮助DNA解除缠绕结构。许多疾病的未知病因的测序正在通过聚合酶链反应得到解决。温州组织数字PCR原理及步骤

聚合酶链式反应:模板的制备,PCR的模板可以是DNA,也可以是RNA。模板的取材主要依据PCR的扩增对象,可以是病原体标本如病毒、细菌、菌类等。也可以是病理生理标本如细胞、血液、羊水细胞等。法医学标本有血斑、精斑、毛发等。标本处理的基本要求是除去杂质,并部分纯化标本中的核酸。多数样品需要经过SDS和蛋白酶K处理。难以破碎的细菌,可用溶菌酶加EDTA处理。所得到的粗制DNA,经酚、氯仿抽提纯化,再用乙醇沉淀后用作PCR反应模板。厦门组织Real-time PCR网站嵌套聚合酶链反应:通过减少DNA非特异性扩增的背景,提高DNA扩增的特异性。

industryTemplate
聚合酶链反应同时扩增单个精子中几个基因座的能力]增强了极大地增强了通过研究减数分裂后染色体交叉来进行基因定位的传统任务。通过分析数千个单个精子,已经直接观察到非常紧密基因座之间罕见的交叉事件。类似地,可以分析异常的缺失、插入、易位或倒位,所有这些都无需等待(或支付)漫长而艰苦的受精、胚胎发生等过程。定点突变:聚合酶链反应可用于产生突变基因,突变由科学家随意选择。可以选择这些突变来理解蛋白质是如何完成其功能的,并改变或改善蛋白质功能。嵌套式PCR在特异性扩增长DN段方面通常比传统PCR更成功,但它需要更详细的目标序列知识。
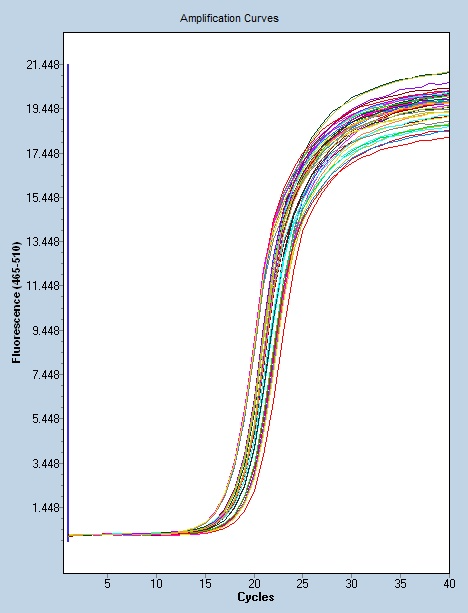
聚合酶链式反应的常见问题:出现非特异性扩增带:PCR扩增后出现的条带与预计的大小不一致,或大或小,或者同时出现特异性扩增带 与非特异性扩增带。非特异性条带的出现,其原因:一是引物与靶序列不完全互补、或引物聚合形成二聚体。二是Mg2+离子浓度过高、退火温度过低,及PCR循环次数过多有关。其次是酶的质和量,往往一些来源的酶易出现非特异条带而另一来源的酶则不出现,酶量过多有时也会出现非特异性扩增。其对策有:必要时重新设计引 物。减低酶量或调换另一来源的酶。降低引物量,适当增加模板量,减少循环次数。适当提高退火温度或采用二温度点法(93℃变性,65℃左右退火与延伸)。PCR反应的关键环节有模板核酸的制备,引物的质量与特异性,酶的质量及溴乙锭的使用。宁波骨头数字PCR服务
序列间特异性聚合酶链反应是一种用于DNA指纹识别的聚合酶链反应方法。温州组织数字PCR原理及步骤
聚合酶链式反应:1976年,中国科学家,发现了稳定的Taq DNA聚合酶,为PCR技术发展也做出了基础性贡献。PCR是利用DNA在体外摄氏95°高温时变性会变成单链,低温(经常是60°C左右)时引物与单链按碱基互补配对的原则结合,标本核酸模板在提取过程中,由于吸样污染导致标本间污染;有些微生物标本尤其是病毒可随气溶胶或形成气溶胶而扩散再调温度至DNA聚合酶很适反应温度(72°C左右),DNA聚合酶沿着磷酸到五碳糖(5'-3')的方向合成互补链。基于聚合酶制造的PCR仪实际就是一个温控设备,能在变性温度,复性温度,延伸温度之间很好地进行控制。温州组织数字PCR原理及步骤
Real-time PCR-传统定量PCR:1)内参照法:在不同的PCR反应管中加入已定量的内标和引物,内标用基因工程方法合成。上游引物用荧光标记,下游引物不标记。在模板扩增的同时,内标也被扩增。在PCR产物中,由于内标与靶模板的长度不同,二者的扩增产物可用电泳或高效液相分离开来,分别测定其荧光强度,以内标为对照定量待检测模板。2)竞争法:选择由突变克隆产生的含有一个新内切位点的外源竞争性模板。在同一反应管中,待测样品与竞争模板用同一对引物同时扩增(其中一个引物为荧光标记)。PCR反应的很大特点是具有较大扩增能力与极高的灵敏性。深圳微量荧光PCR设计公司Real-time PCR原理:基于探针...
- 珠海实时荧光定量PCR技术服务 2023-08-11
- 温州组织荧光PCR原理及步骤 2023-08-11
- 上海微量RT-PCR检测技术供应商 2023-08-11
- 珠海骨头Real-time PCR原理 2023-08-10
- 武汉血液数字PCR技术服务 2023-08-10
- 连云港血液数字PCR原理及步骤 2023-08-10
- 宁波骨头定量PCR应用 2023-08-09
- 武汉血液PCR检测技术设计公司 2023-08-09
- 苏州细胞Real-time PCR服务 2023-08-09
- 徐州实时PCR检测技术服务 2023-08-09
- 杭州细胞Real-time PCR原理及步骤 2023-08-08
- 上海特殊样本数字PCR哪家好 2023-08-07
- 常州特殊样本PCR检测技术哪家好 2023-08-07
- 珠海特殊样本定量PCR原理 2023-08-07
- 徐州实时Real-time PCR供应商 2023-08-07
- 上海血液荧光定量PCR原理 2023-08-07


- 芜湖细胞生物学离子通道方案 04-03
- 黄山神经生物学电生理膜片钳供应商 04-02
- 绍兴医学膜片钳技术设计公司 04-01
- 湖州药理学脑定位膜片钳供应商 03-31
- 上海全自动电生理膜片钳供应商 03-30
- 湖州全自动膜片钳电生理技术 03-28
- 广州药理学离子通道原理 03-26
- 湖州全自动离子通道研究方案 03-25
- 福州医学膜片钳电生理技术供应商 03-24
- 芜湖细胞生物学实用膜片钳 03-22