MOG,英文全名Myelinoligodendrocyteglycoprotein,中文名髓鞘少突胶质细胞糖蛋白,髓鞘的一种微量成分,属于免疫球蛋白超家族成员之一。t也是特定表达于***系统(CNS)的自身抗原,诱导多发性硬化症的原发性脱鞘特征。MOG(35-55)是髓鞘少突胶质细胞糖蛋白的免疫优势表位,能够诱导强烈的T细胞和B细胞应激反应,具高度致脑炎性,能够诱导啮齿类动物的实验性白身免疫性脑脊髓炎(EAE)模型。EAE是**普遍的MS动物模型,具有MS许多的临床和病理生理学特征。单次注射MOG(35-55)能够产生一种复发-缓解型神经性疾病,表现出大量斑块状脱髓鞘病症。1-甲基-4-苯基-1,.2,3,6-四氢吡啶(MPTP)诱导的多巴胺神经元损伤模型,免疫接种MOG(35-55)能抑制该神经元的白发再生功能。EAE具有复杂的神经药理学特征,许多目前已用或即将使用的MS药物得以开发、测试或验证,基于EAE研究。山西大鼠eae模型实验外包

在EAE动物模型中,科学家们能够观察到一系列与多发性硬化症(MS)极为相似的炎症和神经损伤过程。这些过程不仅包括免疫细胞的浸润和激发,还涉及神经纤维的脱髓鞘病变以及神经元的损伤和死亡。通过观察EAE动物模型中的这些病理变化,科学家们能够更加直观地了解MS在人体内的发生机制,从而更加深入地探索疾病的本质。同时,这些观察结果也为科学家们提供了研究MS的新思路和新方向,有助于推动MS的疗愈和研究不断取得新的进展。因此,EAE动物模型在揭示MS病理过程方面发挥着重要作用,为科学家们深入研究这一复杂疾病提供了有力的工具。安徽靠谱的eae模型如何构建EAE模型组小鼠脊髓中均出现髓鞘结构松散,密度降低等髓鞘脱失情况。
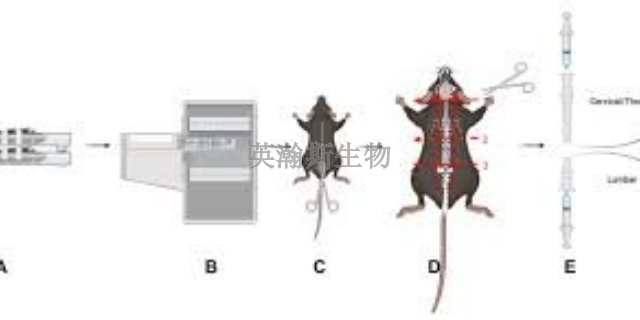
通过对EAE动物模型的基因表达分析,科学家们得以进一步深入了解多发性硬化症(MS)的遗传背景。这一分析过程涉及对模型动物体内基因表达水平的定量和定性研究,通过对比正常动物与EAE模型动物的基因表达差异,科学家们能够识别出与MS发病相关的关键基因和基因网络。这些基因可能涉及免疫调节、神经保护或修复等多个方面,它们的异常表达可能与MS的发病风险、疾病进程以及疗愈效果密切相关。因此,对EAE动物模型进行基因表达分析不仅有助于揭示MS的遗传机制,还为开发针对特定基因靶点的疗愈方法提供了新的思路和方向。这一研究领域的进展将有助于我们更深入地认识MS这一复杂疾病,为未来的疗愈和预防策略提供有力支持。
EAE动物模型,全称为实验性变形反应性脑脊髓炎动物模型,是神经科学研究领域中的一种重要工具。该模型通过模拟多发性硬化症(MS)等神经系统疾病的病理过程,为科学家们提供了一个独特的实验平台,使他们能够深入研究这些疾病的发病机制、病理变化以及疗愈策略。EAE动物模型不仅可以帮助科学家们揭示MS等疾病的发病机理,还可以为开发新的疗愈方法和药物提供重要线索。通过调控模型动物的免疫反应、观察神经系统的再生和修复过程,科学家们可以评估不同疗愈方法的疗效,为MS患者的疗愈提供更为精细和个性化的方案。因此,EAE动物模型在神经科学研究领域具有广泛的应用前景和深远的意义。EAE能再现MS的很多临床和病理特征。
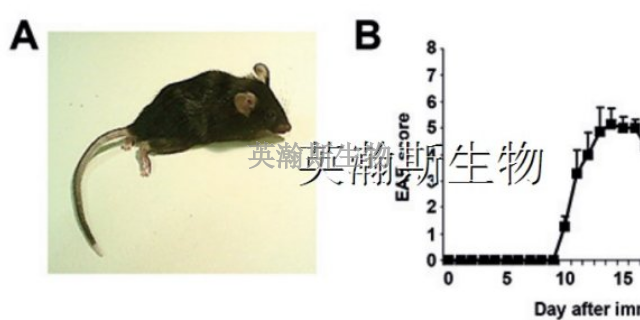
EAE模型的被动转移实验是研究其发病机制的**直接证据,也是研究EAE的***及预防措施的良好模型。将抗原***的PLP特异性T细胞转输给同一品系的正常大鼠或小鼠,也可引起EAE。MBP特异性自身反应性T细胞在MS的发病机制中也起着关键作用,T细胞必须先在外周活化,通过血管内皮细胞进入CNS才能致病。EAE的神经症状通常根据Kono等提出的标准分为5级。0级:无任何临床症状;1级:动物尾巴无力,2级:尾部无力+肢体无力,3级:肢体轻度麻痹,4级:肢体严重麻痹,被动翻身后不能复原;5级:濒死状态或死亡。EAE模型的发生也存在动物性别差异。黑龙江真实的eae模型实验外包
NBP和BMSCs联合可有效缓解EAE模型小鼠的症状。山西大鼠eae模型实验外包
比较不同的神经功能损伤评分标准对小鼠实验性自身免疫性脑脊髓炎(EAE)运动功能障碍评估的效能。方法:应用MOG35-55多肽加完全福氏佐剂乳化后免疫20只C57BL/6小鼠,复制EAE小鼠模型,并使用3种不同的评分标准(Kono's5分法、Hooper's7分法、Weaver's15分法)观察和评估实验动物的发病情况,对实验小鼠在发病初期、高峰期的神经功能障碍进行定量的功能损伤评价。结果:3种评分标准比较,在发病初期,15分法和7分法评估神经损伤症状的敏感性相当,比5分法高;高峰期,以症状评分与病理评分的相关性程度来比较3种评分法的效度,15分法效度比较高,7分法次之。结论:Weaver's15分法评价EAE模型神经功能损伤症状,具有明显的优势,推荐作为今后EAE研究的优先评分法。山西大鼠eae模型实验外包