CD34抗体是一种特异性识别CD34分子的单克隆抗体,在生物科研领域具有重要的应用价值。CD34是一种高度糖基化的跨膜蛋白,主要表达于造血干细胞、祖细胞以及血管内皮细胞的表面,因此被范围广认为是干细胞和血管相关研究的重要标志物。在干细胞研究中,CD34抗体是分离和鉴定造血干细胞的关键工具。通过流式细胞术或免疫磁珠分选技术,研究人员可以利用CD34抗体从复杂的细胞混合物中富集CD34阳性细胞群体,从而研究这些细胞在造血、自我更新和分化中的功能及其调控机制。此外,CD34抗体还被用于研究干细胞的微环境(niche)及其在组织再生中的作用。通过抗体工程技术,可以设计双特异性抗体以实现多功能应用。Whitlow 接头单克隆抗体
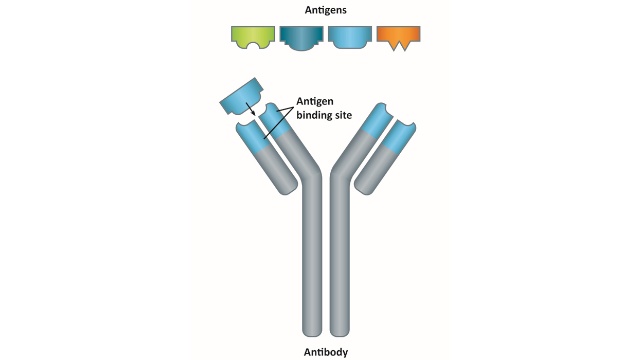
IgA抗体是一种特异性识别免疫球蛋白A(IgA)的单克隆或多克隆抗体,范围广应用于生物科研领域。IgA是黏膜免疫系统中的主要免疫球蛋白,在呼吸道、消化道和泌尿生殖道等黏膜表面起重要保护作用。它以单体形式存在于血清中,或以二聚体形式存在于分泌液中(称为分泌型IgA,sIgA),能够通过中和病原体、阻止其黏附和侵入来发挥免疫防御功能。在免疫学和微生物学研究中,IgA抗体常用于酶联免疫吸附试验(ELISA)、Western blot、免疫荧光染色和免疫组化等技术,用于检测IgA的表达水平及其在黏膜免疫中的作用。例如,在感ran或疫苗接种研究中,该抗体可用于评估黏膜表面IgA的生成动态及其对病原体的中和能力。此外,IgA抗体还被用于研究过敏反应、自身免疫疾病和炎症性肠病中的分子机制。由于其高特异性和在黏膜免疫中的重要地位,IgA抗体已成为免疫学和黏膜免疫研究领域中的重要工具。Whitlow 接头单克隆抗体抗体的表位作图技术有助于解析抗原-抗体相互作用机制。
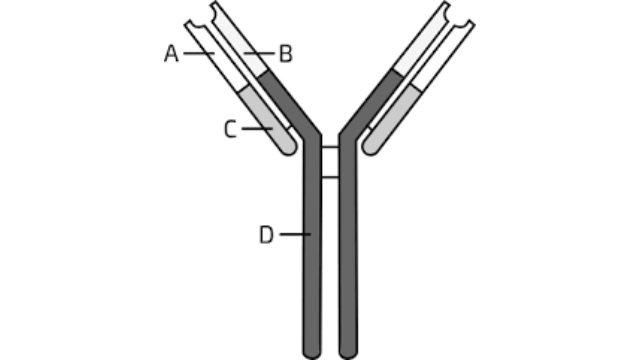
中和抗体是一类能够特异性结合病原体(如病毒、细菌或***)并阻断其生物活性的抗体。在生物科研领域,中和抗体的研究具有重要意义,尤其是在病毒学和免疫学研究中。通过结合病原体的关键区域(如病毒表面的刺突蛋白),中和抗体可以阻止病原体与宿主细胞的相互作用,从而抑制其感ran能力。科研人员通常利用单克隆抗体技术或噬菌体展示技术筛选和开发高特异性的中和抗体,这些抗体不仅可用于研究病原体的感ran机制,还可为开发抗病毒策略提供重要工具。此外,中和抗体还被范围广应用于疫苗研发和免疫应答研究,帮助科学家更好地理解宿主免疫系统如何识别和清理病原体。在实验室中,中和抗体的活性通常通过体外中和实验进行评估,例如利用假病毒系统或细胞感ran模型。这些研究为探索新型治*方法和预防策略奠定了坚实基础。
补体结合抗体是一类能够激*补体系统的抗体,在生物科研中具有重要的研究价值。补体系统是免疫系统的重要组成部分,通过一系列级联反应参与病原体清理、免疫复合物降解以及炎症反应调控。补体结合抗体通常属于IgM或IgG类,其Fc段能够与补体成分C1q结合,从而启动经典补体激*途径。科研人员通过研究补体结合抗体的特性,可以深入探索补体系统的激*机制及其在免疫应答中的作用。例如,在病原体感ran模型中,补体结合抗体的能力直接影响病原体的清理效率;在自身免疫研究中,补体结合抗体与免疫复合物的相互作用也被范围广关注。此外,补体结合抗体的研究还为开发新型免疫调节策略提供了理论支持。通过体外实验,科学家可以利用补体结合抗体研究补体激*的动态过程,揭示其在细胞溶解、炎症信号传导等生物学过程中的具体功能。这些研究为理解免疫系统的复杂调控网络提供了重要线索。抗体的冷冻保存技术能够长期维持其活性和稳定性。
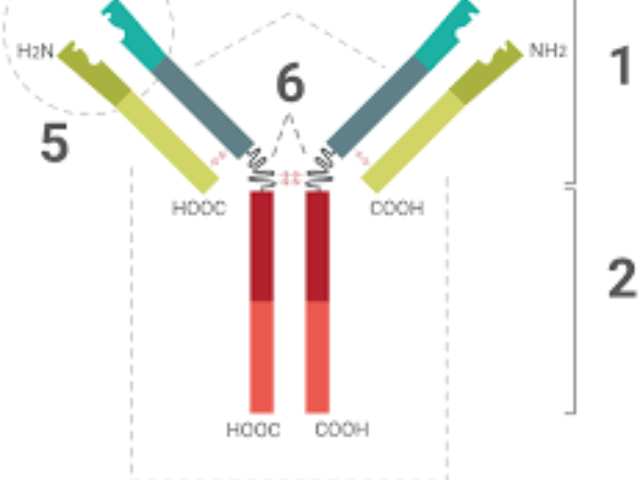
血管内皮生长因子抗体(VEGF抗体)是一种特异性识别血管内皮生长因子(VEGF)的单克隆或多克隆抗体,范围广应用于生物科研领域。VEGF是一种重要的血管生成因子,在血管生成、内皮细胞增殖、迁移和存活中起关键作用。它通过与VEGF受体(VEGFR)结合,激*PI3K/Akt、MAPK和PLCγ等信号通路,促进血管生成和血管通透性增加。在血管生物学和**生物学研究中,VEGF抗体常用于酶联免疫吸附试验(ELISA)、Western blot、免疫荧光染色和免疫组化等技术,用于检测VEGF的表达水平及其在血管生成和**微环境中的作用。例如,在**血管生成研究中,该抗体可用于评估VEGF的表达动态及其对血管内皮细胞功能的影响。此外,VEGF抗体还被用于研究缺血性疾病、炎症和发育生物学中的血管生成机制。由于其高特异性和在血管生成调控中的重要地位,VEGF抗体已成为血管生物学和**研究领域中的重要工具。重组抗体因其可定制性和高稳定性,广泛应用于生物科研。抗体免疫荧光原位杂交
抗体在病原体入侵机制研究中用于阻断关键相互作用。Whitlow 接头单克隆抗体
组蛋白H3抗体是一种重要的研究工具,主要用于检测组蛋白H3的表达及其修饰状态。组蛋白H3是核小体的重要组成部分之一,与DNA紧密结合,参与染色质结构的形成和基因表达的调控。组蛋白H3的翻译后修饰(如甲基化、乙酰化、磷酸化等)在表观遗传调控中起着关键作用,这些修饰可以影响染色质的开放程度,从而调控基因的转录活性。在研究中,组蛋白H3抗体范围广应用于染色质免疫共沉淀(ChIP)、WesternBlot、免疫荧光等技术中,用于研究基因表达调控、染色质重塑以及细胞分化、增殖等生物学过程。例如,通过检测组蛋白H3的特异性修饰(如H3K4me3、H3K27ac等),可以揭示特定基因启动子或增强子的活性状态。此外,组蛋白H3抗体还被用于研究aizheng、发育生物学和干细胞领域,帮助科学家探索表观遗传机制在疾病发生和发展中的作用。选择高特异性和灵敏度的组蛋白H3抗体对实验结果的准确性和可靠性至关重要。 Whitlow 接头单克隆抗体