宿主蛋白残留检测试剂盒的选择通常基于药物开发的阶段。在早期阶段,通用型宿主蛋白残留检测试剂盒通常足够满足监管要求。这些试剂盒通常具有guang fan活性的抗体,可以覆盖多种细胞系产生的HCP。然而,在后期阶段,特定型和工艺平台型的宿主蛋白残留检测试剂盒可能更适合,因为它们可以提供更高的特异性,满足临床试验中的特殊需求。在选择宿主蛋白残留检测试剂盒时,需要考虑稳定性、特异性、准确性和灵敏度。此外,在方法开发中,科学家们通常会使用正交方法,如2D蛋白质印迹法和质谱技术,来提高HCP覆盖范围的可靠性。这些方法的综合应用可以确保宿主蛋白残留检测试剂盒的高质量和稳定性。总的来说,宿主蛋白残留检测试剂盒的选择和优化是生物制药领域中一个复杂而关键的任务。通过合适的选择和科学的方法优化,生物制药公司可以确保产品质量,满足监管标准,从而为患者提供安全有效的药物。更多关于HCP相关产品信息,欢迎咨询上海曼博生物!细胞宿主蛋白残留检测试剂盒的原理。湖州申科宿主蛋白残留检测试剂盒覆盖率
宿主蛋白残留检测试剂盒的应用有助于推动生物制药行业的标准化和规范化发展。通过统一的检测方法和标准,不同企业和研究机构之间能够更好地比较和交流检测结果。这对于提高整个行业的质量水平,促进技术创新和合作具有重要意义。例如,行业协会和专业组织会制定宿主蛋白残留检测的相关标准和指南,为试剂盒的研发和应用提供指导,推动生物制药行业的健康发展。未来,宿主蛋白残留检测试剂盒有望与其他先进技术相结合,实现更高效、检测。例如,与人工智能和大数据分析技术结合,能够对大量的检测数据进行快速分析和挖掘,为生物制药工艺的优化提供更有价值的信息。同时,随着生物技术的不断进步,新的宿主蛋白残留检测标志物的发现和应用,也将为试剂盒的发展带来新的机遇和挑战。我们期待在未来,宿主蛋白残留检测试剂盒能够不断创新和完善,为生物制药行业的发展和人类健康事业做出更大的贡献。现货供应宿主蛋白残留检测试剂盒检测方法Biogenes宿主蛋白残留检测试剂盒购买咨询上海曼博生物。
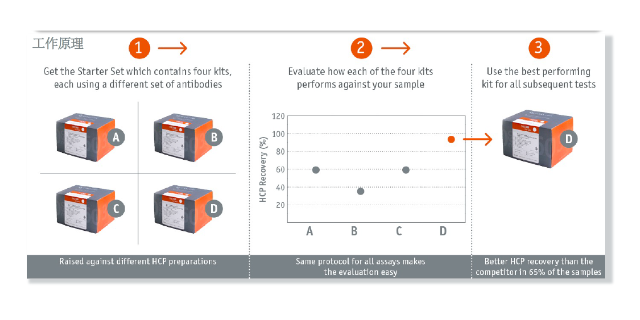
BioGenes公司在这一领域具有xianzhu的经验。他们开发了一种增强版通用CHO宿主蛋白残留检测试剂盒,相比其他商业化通用型宿主蛋白残留检测试剂盒,它展现了明显的优势。该套试剂盒不仅提供了A~D型四种选择,每种试剂盒都使用不同的抗体组,覆盖了guangfan的抗原,而且在特异性、灵敏度和回收率等方面都表现出色。HCP标准品:·从CHO-S和CHO-K1的细胞培养上清液中收集,并分批储存在-70°C下·根据BioGenesSOP进行纯化,并进行质量鉴定,Zui终制成为标准品母液CHO宿主蛋白标准品·通过根据BioGenes质量准则进行放行测试,确保批次一致性。
宿主蛋白残留检测试剂盒的市场需求持续增长。随着生物制药行业的蓬勃发展,对药品质量的要求越来越高,推动了对高质量检测试剂盒的需求。同时,监管机构对生物制品的审批也越来越严格,要求企业提供更专业、准确的宿主蛋白残留检测数据。这促使试剂盒制造商不断加大研发投入,提高产品性能,以满足市场的需求。例如,一些国民度高的试剂盒制造商不仅在国内市场占据重要地位,还积极拓展国际市场,为全球生物制药行业提供的检测解决方案。宿主蛋白残留检测试剂盒的正确使用方法。

在特异性方面,这些试剂盒通过二维凝胶电泳和相应的A~D型试剂盒的抗体进行免疫印迹,确定了所有四种测定对抗原的高特异性。这意味着在不同的制药项目中,这些试剂盒都能提供高度特异性的宿主蛋白残留检测服务。在灵敏度方面,这些试剂盒的检测下限在0.5~1.0 ng/mL之间,定量下限为2~3 ng/mL,工作范围为2~100 ng/mL。这种高度的灵敏度保证了在低浓度下也能够准确地检测到宿主蛋白残留。而在回收率方面,这种增强版的宿主蛋白残留检测试剂盒已经在大量模拟CHO-HCP样本的基础上进行了guang fan测试。通过与其他常用试剂盒进行对比,这套试剂盒的回收率明显更高,这意味着它在实际样本中的应用更为可靠。更多关于Biogenes相关产品信息,欢迎咨询上海曼博生物!HCP细胞宿主蛋白残留检测试剂盒有哪些品牌?BSA宿主蛋白残留检测试剂盒灵敏度
对于每种类型,Biogenes抗体储备足以生产2000-3000个ELISA试剂盒。湖州申科宿主蛋白残留检测试剂盒覆盖率
此外,BioGenes的ELISA试剂盒还通过了严格的验证和认证,符合美国和欧洲药品监管机构的标准。生物制药企业在使用这款试剂盒时,可以更加放心,因为他们知道自己所使用的是经过quanwei认证的产品,能够为产品的合规性提供有力支持。总的来说,BioGenes的通用360-HCPELISA试剂盒不仅是一款技术先进的产品,更是一项为生物制药企业提供quanfangwei支持的解决方案。有了这款试剂盒,生物制药企业可以更加高效、准确地进行HCP残留的监测和控制,确保产品的质量和安全性。BioGenes的团队将继续致力于研发更先进的产品和服务,为生物制药行业的发展贡献自己的力量。更多关于BioGenes的产品信息,欢迎咨询上海曼博生物!湖州申科宿主蛋白残留检测试剂盒覆盖率
BioGenes的增强版通用CHO宿主蛋白残留检测试剂盒不仅具备良好的特异性和灵敏度,而且在回收率方...
【详情】当涉及到生物制药的质量控制时,宿主蛋白残留检测是一个至关重要的环节。而在不同的制药阶段,选择合适...
【详情】在特异性方面,这些试剂盒通过二维凝胶电泳和相应的A~D型试剂盒的抗体进行免疫印迹,确定了所有四种测定...
【详情】在特异性方面,这些试剂盒通过二维凝胶电泳和相应的A~D型试剂盒的抗体进行免疫印迹,确定了所有四种测定...
【详情】BioGenes公司在这一领域具有xianzhu的经验。他们开发了一种增强版通用CHO宿主蛋白残留检...
【详情】BioGenes的增强版通用CHO宿主蛋白残留检测试剂盒不仅具备良好的特异性和灵敏度,而且在回收率方...
【详情】当涉及到生物制药的质量控制时,宿主蛋白残留检测是一个至关重要的环节。而在不同的制药阶段,选择合适的H...
【详情】在性能研究方面,Biogenes提供了完善的表征服务,确保为客户推荐Zui佳性能的宿主蛋白残留检测试...
【详情】BioGenes的试剂盒不仅具备高度特异性,还在灵敏度上有着出色的表现。通过考马斯染色和2DWest...
【详情】宿主蛋白残留检测试剂盒的选择需要综合考虑多个因素。首先是试剂盒的检测性能,包括灵敏度、特异性和准确性...
【详情】宿主蛋白残留检测试剂盒在保障公共健康方面发挥着间接但重要的作用。通过确保生物制药产品的质量和安全性,...
【详情】BioGenes是一家提供定制免疫分析和抗体开发的quanfangwei服务提供商,对质量和服务有着...
【详情】