小鼠在子宫内膜异位症模型建立上的研究子宫内膜异位症是一种因子依赖性、出血性、炎症性和遗传性疾病,它是有活性的子宫内膜在被覆内膜的宫腔和子宫以外的部位生长、浸润,从而引发疼痛、结节、月经紊乱以及不孕症等疾病。为了探索改善子宫内膜异位症的方法,常采用小鼠建立子宫内膜异位症动物模型时,使用比较多的是包括SCID小鼠、裸鼠在内的免疫缺陷小鼠。采用SCID小鼠或裸鼠进行子宫内膜异位症的建模,便于实验研究。子宫内膜异位症(内异症)动物模型的建立可以有自发、异体移植和诱发3种主要模式。利用子宫内膜异位症模型,我们可以测试新药物对疾病的改善效果。江西推荐的子宫内膜异位症模型实验外包
子宫内膜异位症模型是研究该疾病发病机理的重要工具,它为我们提供了一个深入探索疾病本质的平台。通过模拟子宫内膜异位症在人体内的发生和发展过程,这一模型使我们能够更直观地观察疾病的病理变化,从而揭示其发病机理。借助这一工具,研究人员可以系统地研究子宫内膜异位症与因子、免疫、遗传等因素之间的关系,进而为疾病的预防和改善提供科学依据。此外,子宫内膜异位症模型还为药物研发提供了重要的实验平台,通过测试新药物在模型中的疗效,我们可以筛选出具有潜在改善价值的药物,为子宫内膜异位症患者带来福音。因此,子宫内膜异位症模型在推动妇科医学的发展和提高患者生活质量方面发挥着不可替代的作用。贵州靠谱的子宫内膜异位症模型是哪家子宫内膜异位症模型为疾病的早期诊断提供了可能性。
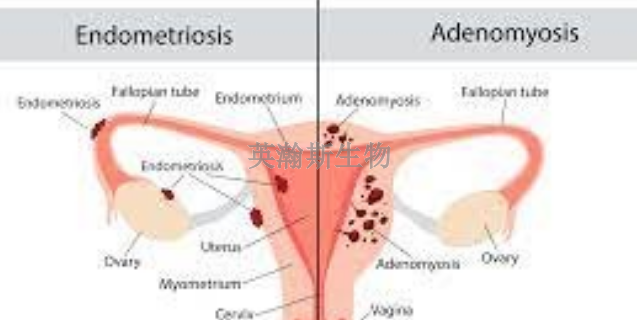
用于子宫内膜异位症模型的动物主要有灵长类动物和啮齿类动物,以及家兔、巴马香猪、鸡胚尿囊膜等。灵长类动物是***与人类相似、能自发形成EM的动物,因此是研究EM比较合适的动物模型。然而, 由于实验动物缺乏、价格昂贵、饲养条件高、成模率低、实验周期长以及伦理学等多种原因限制了灵长类动物EM模型实验的研究。啮齿类动物由于价格便宜、易于获得、成模率高,被普遍采用。啮齿类动物包括大鼠和小鼠,其中免疫缺陷小鼠可进行异体移植[5,6,7],直接接受人体子宫内膜的移植,并且保留其原有特性,更接近人类疾病的病理变化,但由于其免疫功能缺陷,不能用来研究机体免疫方面的改变,且不能耐受多次手术和**检验。近年来,荧光EM小鼠模型的应用日益普遍,荧光动物模型是体内无创观察模型,其主观性小,病灶定位准确,能动态无损伤量化观察病灶生长情况,操作简单[8],但荧光表达时间有限,比较长只为4周,缺乏定量种植及观察标准。
有研究者使用SCID小鼠进行了子宫内膜异位症模型的移植建立研究,也有研究者使用裸鼠异体移植法及***成像技术,构建人子宫内膜异位症的可示踪模型。1、构建裸鼠及SCID小鼠子宫内膜异位症模型有研究者构建了子宫内膜异位症裸鼠及SCID小鼠动物模型,比较在位及异位来源的人子宫内膜组织对移植效果的影响,为内异症的药物治疗研究提供有利的动物模型基础[1]。方法取性成熟BALB/c-nu/nu裸鼠及SCID小鼠各30只,通过皮下移植法,将在位及异位子宫内膜移植到下腹部皮下,定期观察异位病灶的大小,术后6周取出病灶,病理学检查。结果发现裸鼠及SCID小鼠均可建立成功的内异症动物模型。其中SCID小鼠的建模成功率较裸鼠更高(86.7%和66.7%),在位子宫内膜组种植的成功率明显高于异位子宫内膜组(100%vs84.2%)。因此SCID小鼠在位内膜皮下种植方法可成功建立内异症研究人员正在不断优化子宫内膜异位症模型,以提高其实验准确性。
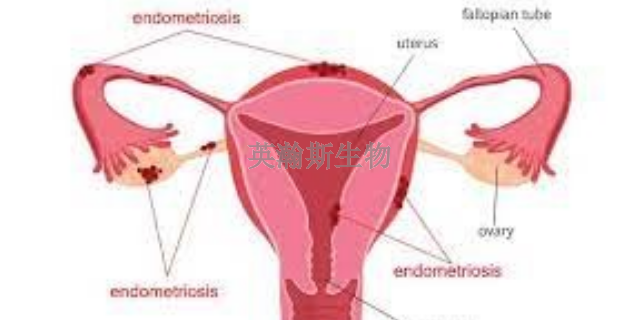
手术移植法是建立子宫内膜异位症动物模型的主要方法*!+'经典的子宫内膜异位症造模方法为将大鼠自体子宫内膜手术移植至腹腔内单一部位#如缝合于腹壁)卵巢表面)子宫直肠陷凹*8+'亦有报道将子宫内膜组织移植于皮下$腹肌与皮下筋膜层之间%#造模成功率与腹腔种植无差异#有内膜固定好#免去手术缝合#操作简单等优点*37!!+'亦有报道皮下注射法造模成功率高于皮下移植法*!%+'但是王宁宁等*!#+报道皮下移植法和皮下注射法在造模成功率和病灶体积无差异'本实验比较腹腔种植)皮下移植和皮下注射#种方法的子宫内膜异位症造模成功率差异无统计学意义$A%"2"&%'种植物组织形态相似#体积大小无明显差异'因此##种造模方法均可以较好的建立大鼠子宫内膜异位症模型'相对于腹腔种植法#皮下移植法无需缝合子宫内膜组织#符合自然黏附原则#避免缝线的异物刺激改变子宫内膜异位症病灶周围的微环通过子宫内膜异位症模型,我们可以研究疾病与环境因素的相互作用。浙江靠谱的子宫内膜异位症模型如何构建
该模型为子宫内膜异位症的诊断和改善提供了新的思路和方法。江西推荐的子宫内膜异位症模型实验外包
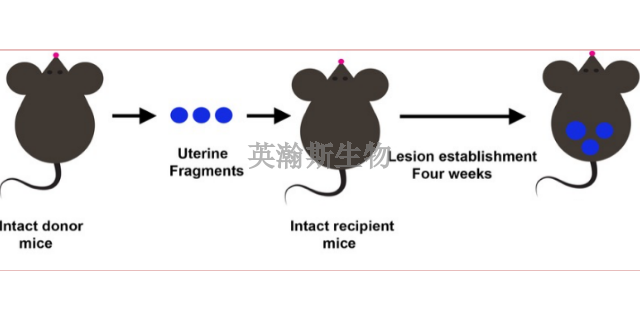
子宫内膜异位症模型同种异体移植法:1.随机取小鼠一只作为捐赠鼠,脱颈椎法处死,仰卧位固定于手术台,腹部酒精消毒后,沿正中线剖开腹腔。找到Y形子宫,小心分别牵出左、右侧子宫,细心分离双侧子宫系膜。2.离断宫角与卵巢,在Y形子宫分叉分别剪断左侧及右侧子宫,放入装有生理盐水的无菌弯盘中,反复漂洗子宫表面的血迹,进一步分离剩余粘附的子宫系膜。将两个子宫角分别放置于两个无菌弯盘中,将它们直接剪成大小均等约1mm×1mm的碎片,并将它们悬浮于生理盐水中。3.将捐赠鼠的子宫按1/2的比例种植于接受鼠腹腔,1只捐赠鼠内膜供应2只接受鼠,用生理盐水悬浮弯盘里的组织碎片。4.随机取一只小鼠作为接受鼠,取脐下偏正中线处的左下腹为进针点,将溶有子宫组织碎片的生理盐水用号针头连同子宫组织块碎片注入接受鼠的腹腔,后放置于鼠笼。江西推荐的子宫内膜异位症模型实验外包