- 品牌
- 司鼎;OriCell
聚合酶链式反应:因为PCR扩增了目的DNA区域,所以PCR可以用于分析极少量的样品。这对于法医检定法,当时只有微量的DNA可作为证据。聚合酶链反应也可用于分析古代DNA那已经有数万年的历史了。这些基于聚合酶链反应的技术已经成功地应用于动物身上,例如四万年前猛犸,以及人类DNA,应用范围从分析埃及木乃伊识别一个俄罗斯沙皇和英国国王理查三世遗体的鉴定。定量聚合酶链反应或者实时聚合酶链反应不要与逆转录-聚合酶链反应方法混淆)允许估计样品中存在的给定序列的量——这种技术通常用于定量确定基因表达的水平。定量PCR是一种已建立的DNA定量工具,用于测量每轮PCR扩增后DNA产物的积累。聚合酶链反应应经常使用带有一次性柱塞和超长移液器吸头的移液器。常州特殊样本RT-PCR检测技术网站
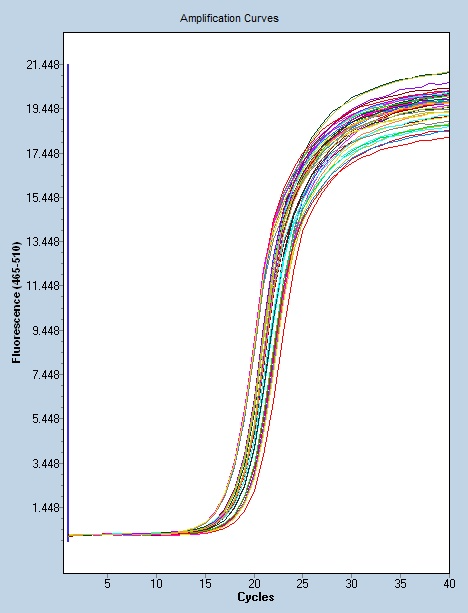
聚合酶链反应的常见问题分析与解决方法:反应缓冲液未完全融化或未充分混匀。确保反应缓冲液融化完全并彻底混匀。引物特异性差。利用BLAST检查引物特异性或重新设计引物。引物量过多。减少反应体系中引物的用量。模板量过多。质粒DNA的用量应<50ng,而基因组DNA则应<200ng。外源DNA污染。确保操作的洁净。阴性对照出现条带:试剂,头,工作台污染。使用全新的试剂和头,对工作台进行清洁。条带大小与理论不符:污染。使用全新的试剂和头,对工作台进行清洁。模板或引物使用错误。更换引物和模板。基因亚型。对研究的基因进行序列分析和BLAST研究。常州特殊样本RT-PCR检测技术网站电子聚合酶链反应用于计算理论聚合酶链反应结果。
绝大多数聚合酶链反应方法依赖于热循环。热循环将反应物暴露于加热和冷却的重复循环中,以允许不同的温度依赖性反应——具体地说,脱氧核糖核酸融化和酶-驱动DNA复制。聚合酶链反应使用两种主要试剂-引物(引物是短的单链DN段,称为寡核苷酸,是目标DNA区域的互补序列)和DNA聚合酶。在PCR反应的步,DNA双螺旋结构的两条链在高温下物理分离,这个过程称为脱氧核糖核酸变性。第二步,降低温度,引物与互补的脱氧核糖核酸序列结合。这两条DNA链就变成了模板,以酶促的方式从构成DNA的自由核苷酸中组装出一条新的DNA链。随着聚合酶链反应的进行,产生的DNA本身被用作复制的模板,启动了一个连锁反应,原始的DNA模板是以指数形式放大。
PCR的反应条件:dNTP浓度过高会加快反应速度,但同时还可以增加碱基的错误掺入率。引物浓度过高会引起错配和非特异性产物扩增。TaqDNA聚合酶浓度过高会引起错配和非特异性产物扩增,低则合成产物量减少。TaqDNA聚合酶无校正功能,掺入错误率达2*E-4个核苷酸,一个30个循环的扩增反应0.1%-0.25%总错误率。在90~95度下可使整个基因组的DNA变性为单链。一般94~95度30~60s。时间过长使TaqDNA聚合酶失活和dNTP破坏增多。DNA很快冷却到40~60度使引物和模板结合。引物长度在15~25时退火温度。聚合酶链式反应的引物与非特异扩增区的序列的同源性不要超过70%。

聚合酶链式:PCR由变性--退火--延伸三个基本反应步骤构成:模板DNA的变性:模板DNA经加热至93℃左右一定时间后,使模板DNA双链或经PCR扩增形成的双链DNA解离,使之成为单链,以便它与引物结合,为下轮反应作准备;模板DNA与引物的退火(复性):模板DNA经加热变性成单链后,温度降至55℃左右,引物与模板DNA单链的互补序列配对结合;引物的延伸:DNA模板--引物结合物在TaqDNA聚合酶的作用下,以dNTP为反应原料,靶序列为模板,按碱基配对与半保留复制原理,合成一条新的与模板DNA 链互补的半保留复制链重复循环变性--退火--延伸三过程,就可获得更多的“半保留复制链”,而且这种新链又可成为下次循环的模板。每完成一个循环需2-4分钟,2-3小时就能将待扩目的基因扩增放大几百万倍。到达平台期(Plateau)所需循环次数取决于样品中模板的拷贝。 PCR技术敏感性高,特异性强,操作简便、快速,在生命科学研究、食品卫生、医疗、法医及环境监测等诸多方面都具有重要的应用价值。聚合酶链式反应准备:PCR所用的酶主要有两种来源:Taq和Pfu,分别来自两种不同的噬热菌。常州特殊样本RT-PCR检测技术网站
多重连接依赖探针扩增允许用单个引物对扩增多个靶标,从而避免多重PCR的分辨率限制。常州特殊样本RT-PCR检测技术网站
聚合酶链式反应:反应的控制:PCR反应的缓冲液 提供合适的酸碱度与某些离子;镁离子浓度 总量应比dNTPs的浓度高,常用1.5mmol/L;底物浓度 dNTP以等摩尔浓度配制,20~200umol/L;TaqDNA聚合酶 2.5U(100ul);引物浓度一般为0.1 ~ 0.5umol/L;反应温度和循环次数;变性温度和时间 95℃,30s;退火温度和时间 低于引物Tm值5 ℃左右,一般在45~55℃;延伸温度和时间 72℃,1min/kb(10kb内);Tm值=4(G+C) +2(A+T);循环次数 :一般为25 ~ 30次。循环数决定PCR扩增的产量。模板初始浓度低,可增加循环数以便达到有效的 扩增量。但循环数并不是可以无限增加的。一般循环数为30个左右,循环数超过30个以后,DNA聚合酶活性逐渐达到饱和,产物的量不再随循环数的增加而增加,出现了所谓的“平台期”。常州特殊样本RT-PCR检测技术网站
Real-time PCR-传统定量PCR:1)内参照法:在不同的PCR反应管中加入已定量的内标和引物,内标用基因工程方法合成。上游引物用荧光标记,下游引物不标记。在模板扩增的同时,内标也被扩增。在PCR产物中,由于内标与靶模板的长度不同,二者的扩增产物可用电泳或高效液相分离开来,分别测定其荧光强度,以内标为对照定量待检测模板。2)竞争法:选择由突变克隆产生的含有一个新内切位点的外源竞争性模板。在同一反应管中,待测样品与竞争模板用同一对引物同时扩增(其中一个引物为荧光标记)。PCR反应的很大特点是具有较大扩增能力与极高的灵敏性。深圳微量荧光PCR设计公司Real-time PCR原理:基于探针...
- 珠海实时荧光定量PCR技术服务 2023-08-11
- 温州组织荧光PCR原理及步骤 2023-08-11
- 上海微量RT-PCR检测技术供应商 2023-08-11
- 珠海骨头Real-time PCR原理 2023-08-10
- 武汉血液数字PCR技术服务 2023-08-10
- 连云港血液数字PCR原理及步骤 2023-08-10
- 宁波骨头定量PCR应用 2023-08-09
- 武汉血液PCR检测技术设计公司 2023-08-09
- 苏州细胞Real-time PCR服务 2023-08-09
- 徐州实时PCR检测技术服务 2023-08-09
- 杭州细胞Real-time PCR原理及步骤 2023-08-08
- 上海特殊样本数字PCR哪家好 2023-08-07
- 常州特殊样本PCR检测技术哪家好 2023-08-07
- 珠海特殊样本定量PCR原理 2023-08-07
- 徐州实时Real-time PCR供应商 2023-08-07
- 上海血液荧光定量PCR原理 2023-08-07


- 绍兴多重免疫荧光用途 11-17
- 黄石组织芯片免疫荧光 11-14
- 东莞多重免疫荧光哪家好 11-12
- 淮南多种位点组织芯片定制 11-11
- 襄阳多种位点组织芯片特点 10-30
- 合肥组织芯片免疫组化哪家好 10-29
- 南京多种位点组织芯片用途 10-28
- 芜湖多种位点组织芯片技术服务 10-27
- 襄阳原位杂交哪家专业 10-26
- 武汉多重免疫荧光哪家好 10-25