我国生物试剂出口政策旨在规范出口秩序,推动产业健康发展,同时保障生物安全与公共卫生安全。国家相关部门,如商务部、国家药品监督管理局等协同监管,依据一系列法规构建政策体系。出口生物试剂必须确保质量符合国际标准以及目标市场要求,生产过程遵循良好生产规范(GMP)等准则。企业需在合法合规前提下开展出口业务,履行各类申报与备案手续。对于不同类型生物试剂,依据其风险程度与应用领域,制定差异化出口管理措施,既助力不错生物试剂拓展国际市场,又严格把控可能存在的风险,维护国家利益与国际声誉。对于生物试剂出口,要提前评估进口国市场需求。昆山细胞培养试剂进出口监管法规
进出口的生物试剂必须符合目标市场的质量与安全标准。在出口环节,产品要多方面满足进口国法规及相关国际标准。以出口欧盟的生物试剂为例,其必须符合欧盟指令与协调标准,通过 CE 认证,该认证涵盖产品安全性、健康影响、环保等多方面评估,只有顺利通过认证机构检测与审核,获得认证证书,产品才能在欧盟市场流通。出口美国则要符合美国食品药品监督管理局(FDA)要求并完成相应注册程序,如医疗器械类生物试剂可能需进行 510 (k) 申请或上市前批准(PMA)等。进口生物试剂时,需确保其符合我国药品、医疗器械等相关法规,例如药品类生物试剂要符合我国药品注册标准,从药品的成分、纯度到稳定性等各方面都有细致规定;医疗器械类生物试剂要通过国内注册或备案,产品的研发、生产、质量控制等环节都要达到对应规范,否则产品将无法顺利通关,更无法进入市场销售,还可能面临召回、处罚等风险。上海港特殊物品进口清关手续生物试剂进口要了解目的国对生物试剂捐赠的相关规定。

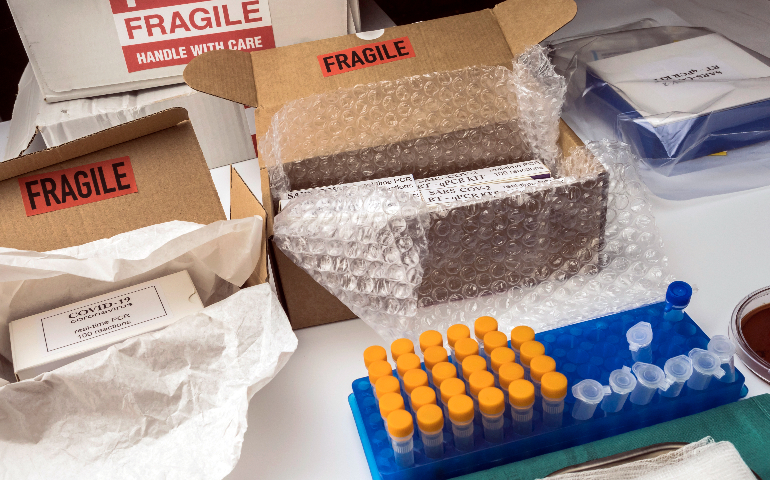
生物试剂出口的包装与标识必须严格遵循国际标准与目标市场法规。包装材料要具备良好防护性能,确保试剂在运输、储存过程中不受损坏,对于有特殊储存要求(如低温、避光)的试剂,包装需采取相应措施维持适宜环境。包装标识应清晰标注产品名称、成分、规格、生产企业、生产日期、有效期、储存条件、使用说明等关键信息,且必须使用目标市场通用语言(如英语,同时可能需翻译为当地语言)。对于危险生物试剂,要依据国际《关于危险货物运输的建议书》等标准,在包装上张贴正确的危险货物标识,以保障运输安全与信息准确传递。
进出口生物试剂都要经过严格检验检疫。出口时,企业要主动向海关与检验检疫部门申报,提供详细的产品信息、生产批次、质量检测报告等资料。检验检疫部门会根据试剂特性和进口国要求,抽检纯度、活性、微生物限度等指标,对可能携带病原体、有害生物因子的试剂进行生物安全检测。进口生物试剂时,同样要接受我国检验检疫部门查验,企业需配合做好货物查验、抽样检测等工作。对于冷链生物试剂,还要满足冷链货物检验检疫要求,确保产品符合国内外检验检疫标准,维护公共卫生安全与市场秩序。对于生物试剂出口,要提前掌握进口国的检疫程序。

进口生物试剂的企业必须具备特定资质。首先,企业需完成对外贸易经营者备案登记,获得合法进出口经营权。若进口药品类生物试剂,应持有有效的药品经营许可证,其仓储、运输等设施要符合药品经营质量管理规范(GSP),确保试剂储存与流通环节质量可控。对于医疗器械类生物试剂进口,企业需依据试剂风险等级,完成医疗器械经营备案或取得医疗器械经营许可证。企业还应配备专业人员,包括熟悉生物试剂法规、质量控制及进口业务流程的管理人员与技术人员,以满足进口业务的专业操作与合规管理需求。对于生物试剂出口,需向进口国提供详细的产品技术资料。昆山细胞培养试剂进出口监管法规
出口生物试剂要确保产品在进口国的合法合规销售。昆山细胞培养试剂进出口监管法规
随着科技发展,新兴技术在生物试剂进出口领域普遍应用。在质量检测方面,基因测序技术用于精确检测生物试剂中 DNA、RNA 等生物分子的序列,能快速准确鉴定试剂的纯度和特性,相比传统检测方法更高效、精细。在运输环节,物联网技术发挥重要作用,通过在冷链运输设备上安装传感器,实时采集温度、湿度等数据,并上传至监控平台,企业可随时掌握运输状态,一旦出现异常能及时采取措施,确保生物试剂在适宜条件下运输。此外,3D 打印技术也开始应用于定制化生物试剂包装,可根据试剂特殊形状和防护需求,快速制作个性化包装,提高包装的适配性和防护效果,助力生物试剂进出口业务的高效发展。昆山细胞培养试剂进出口监管法规